摘要gydF4y2Ba
发育开始时的一个关键事件是卵母细胞到胚胎转变过程中收缩肌动球蛋白皮层的激活gydF4y2Ba1克ydF4y2Ba,gydF4y2Ba2 gydF4y2Ba,gydF4y2Ba3.gydF4y2Ba.在这里我们报道的发现,在gydF4y2Ba秀丽隐杆线虫gydF4y2Ba在卵母细胞中,肌动球蛋白皮层的激活由数千个富含F-actin、N-WASP和ARP2/3复合物的短命蛋白凝聚体的出现支持gydF4y2Ba4gydF4y2Ba,gydF4y2Ba5gydF4y2Ba,gydF4y2Ba6gydF4y2Ba,gydF4y2Ba7gydF4y2Ba,gydF4y2Ba8gydF4y2Ba形成活性微乳液。对单个皮质凝聚体动力学的相像分析表明,凝聚体最初生长,然后在完全溶解之前过渡到分解。我们发现,与凝结物通过扩散增长相反gydF4y2Ba9gydF4y2Ba,皮层凝聚体的生长动态是化学驱动的。值得注意的是,相关的化学反应服从质量作用动力学,控制成分和大小。我们认为由此产生的凝析液具有动力不稳定性gydF4y2Ba10gydF4y2Ba抑制活性微乳液的粗化gydF4y2Ba11gydF4y2Ba,确保反应动力学独立于冷凝液大小,并防止失控的f -肌动蛋白成核过程中形成的第一个皮层肌动蛋白网。gydF4y2Ba
主要gydF4y2Ba
形态发生涉及在细胞肌动球蛋白皮质层内产生的力gydF4y2Ba1克ydF4y2Ba.不恰当的皮质组织会导致关键的细胞和发育过程受损,从早期的卵母细胞减数分裂到随后的每一次细胞分裂gydF4y2Ba12gydF4y2Ba.在卵母细胞的减数分裂成熟过程中,肌动球蛋白皮层由不活跃和不收缩转变为活跃和产生张力gydF4y2Ba2 gydF4y2Ba,gydF4y2Ba3.gydF4y2Ba.这种转变可以产生一系列肌动球蛋白皮质结构和动力学,包括小鼠卵母细胞中的肌动蛋白帽gydF4y2Ba13gydF4y2Ba,在海星卵母细胞中的肌动蛋白峰值gydF4y2Ba14gydF4y2BaRho激活波和f -肌动蛋白聚合波gydF4y2Ba非洲爪蟾蜍gydF4y2Ba15gydF4y2Ba.组织第一个活跃的肌动球蛋白皮层需要各种皮层成分的募集和组装以及肌动蛋白丝的聚合gydF4y2Ba4gydF4y2Ba.这些过程必须协调整个细胞表面,以产生一个统一的肌动球蛋白皮质层。在这里,我们想知道在卵母细胞减数分裂成熟过程中,活跃的、产生张力的肌动球蛋白皮质是如何形成的。gydF4y2Ba
肌动球蛋白皮层激活gydF4y2Ba
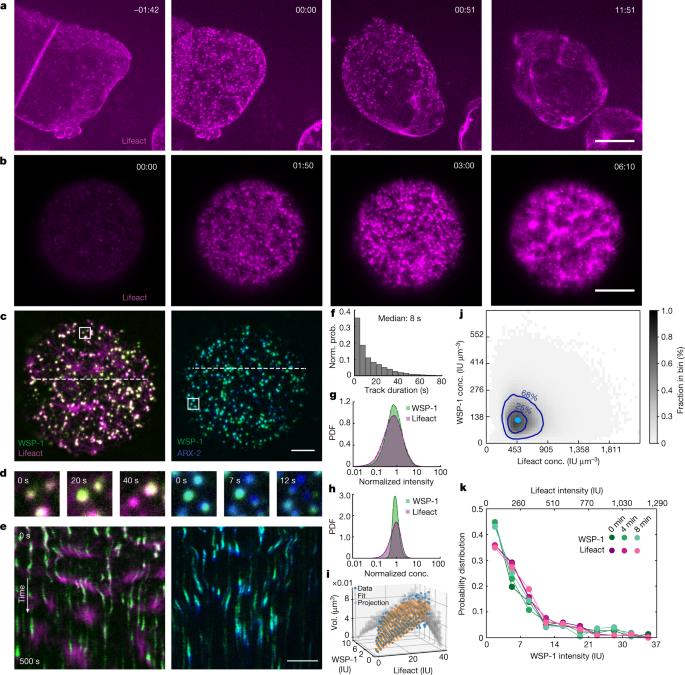
雌雄同体线虫gydF4y2Ba秀丽隐杆线虫gydF4y2Ba是研究卵母细胞成熟过程中肌动球蛋白皮质形成的主要系统吗gydF4y2Ba16gydF4y2Ba,gydF4y2Ba17gydF4y2Ba,gydF4y2Ba18gydF4y2Ba.在gydF4y2Ba秀丽隐杆线虫gydF4y2Ba,减数分裂和卵母细胞成熟的开始与排卵和受精一致gydF4y2Ba16gydF4y2Ba,gydF4y2Ba18gydF4y2Ba.卵母细胞在雌雄同体的母体内受精,因为它们穿过含有精子的器官——精囊gydF4y2Ba16gydF4y2Ba.为了了解卵母细胞成熟过程中第一个肌动球蛋白皮层的形成是如何安排的,我们在卵母细胞成熟过程中观察到f -肌动蛋白gydF4y2Ba秀丽隐杆线虫gydF4y2Ba含有Lifeact::mKate2的卵母细胞。我们观察到,在母体内受精之前,卵母细胞皮层层未发育,只有稀疏的丝状肌动蛋白存在(图2)。gydF4y2Ba1gydF4y2Ba(左)。相比之下,受精后不久,质膜下出现了高度动态和密集的肌动球蛋白皮质层(图2)。gydF4y2Ba1gydF4y2Ba右图和补充视频gydF4y2Ba1克ydF4y2Ba).重要的是,我们发现卵母细胞中的肌动球蛋白皮层激活通过一个持续约10分钟的中间阶段发生,导致一个动态和收缩的肌动球蛋白皮层层,并以第一极体的挤压结束gydF4y2Ba19gydF4y2Ba(补充视频gydF4y2Ba1克ydF4y2Ba).引人注目的是,这个中间阶段的特点是在皮层层短暂出现数千个富f -肌动蛋白凝聚体(图。gydF4y2Ba1gydF4y2Ba).这里我们使用术语冷凝指的是由集体分子相互作用维持的特定分子成分的密集组装。f -肌动蛋白及其成核物先前已被证明可以形成生物分子凝聚体,并提供了类似液体性质的证据gydF4y2Ba5gydF4y2Ba,gydF4y2Ba6gydF4y2Ba,gydF4y2Ba7gydF4y2Ba,gydF4y2Ba8gydF4y2Ba.我们观察到的富f -肌动蛋白凝聚体是高度动态的,本质上不稳定。它们随机出现,大约10秒后消失。gydF4y2Ba
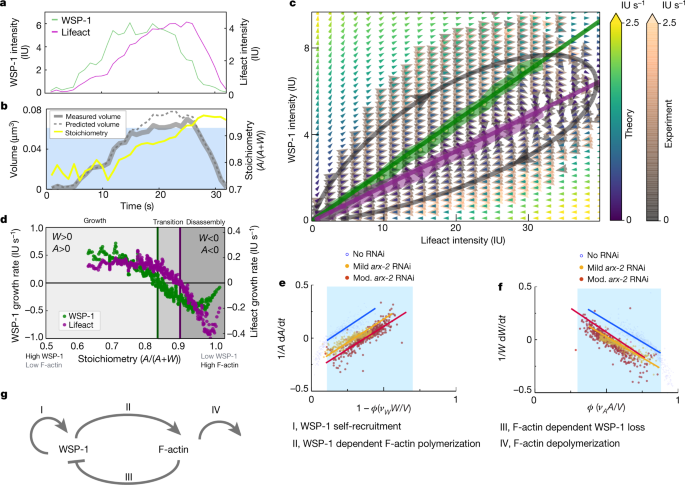
一个gydF4y2Ba,卵母细胞向胚胎转变的宫内显微镜图像gydF4y2Ba秀丽隐杆线虫gydF4y2Ba在不同的受精时间(min:s)。洋红色的F-actin (Lifeact::mKate);比例尺,10 μm (gydF4y2Baa, b, c, egydF4y2Ba).gydF4y2BabgydF4y2Ba,正在成熟的分离卵母细胞的TIRF图像。在两个例子中(gydF4y2Ba一个gydF4y2Ba而且gydF4y2BabgydF4y2Ba),一个可收缩的皮层形成(最右边的图像),这一阶段的特征是出现富含f -肌动蛋白的短命动态凝聚体(中间的两幅图像)。gydF4y2BacgydF4y2Ba,皮层凝聚物的TIRF图像。内生的wasp -1::GFP为绿色(左),内生的ARX-2::mCherry为蓝色(右)。gydF4y2BadgydF4y2Ba,凝析物的组成动力学分布在各自的白框内gydF4y2BacgydF4y2Ba随着时间的推移,揭示了相邻凝聚体在瞬时动力学上的差异。gydF4y2BaegydF4y2Ba图中白色虚线所示的凝析动力学图gydF4y2BacgydF4y2Ba.gydF4y2BafgydF4y2Ba,归一化概率(Norm。冷凝液寿命的问题。gydF4y2BaggydF4y2Ba,gydF4y2BahgydF4y2Ba, Lifeact::mKate(品红)和wp -1::GFP(绿色)强度(gydF4y2BaggydF4y2Ba)和浓度(conc.) (gydF4y2BahgydF4y2Ba)凝聚体内。gydF4y2Ba我gydF4y2Ba凝聚体体积(Vol.)的测量(蓝色)基于皮质凝聚体具有球形的假设,并根据体积对分子含量的依赖性计算(橙色)gydF4y2Ba\ ({v} _{一}+ {v} _ {W} W \)gydF4y2Ba.gydF4y2BajgydF4y2Ba,来自9个卵母细胞的36,930个凝聚体中的凝聚体中的f -肌动蛋白和wasp -1的瞬时浓度。这里68%和25%的瞬时凝析液浓度分别落在外部和内部深蓝色等高线内。浅蓝点为对照组卵母细胞中优先维持的wasp -1和F-actin浓度对的峰值。gydF4y2BakgydF4y2Ba, sp -1::GFP(绿线)和Lifeact::mKate(洋红色线)归一化概率密度函数;在卵母细胞成熟后的0、4和8 min,凝析液的综合强度相似。gydF4y2Ba
我们接下来着手研究这些瞬态富f -肌动蛋白凝聚物的性质。为了更好地观察它们的动态,我们利用了从母体分离出来的卵母细胞在没有受精的情况下也能成熟这一事实gydF4y2Ba20.gydF4y2Ba.这使我们能够开发一种全内反射荧光(TIRF)测定方法gydF4y2Ba21gydF4y2Ba在高倾斜和叠层光学片(HILO)条件下用于成像细胞膜附近的细胞结构(图。gydF4y2Ba1 bgydF4y2Ba).这使得在高空间和时间分辨率下对分离的卵母细胞中肌动球蛋白皮质形成进行定量研究成为可能gydF4y2Ba2 gydF4y2Ba).f -肌动蛋白聚合由成核途径成员组织,如N-WASP和ARP2/3复合体,以及拉长子FormingydF4y2Ba22gydF4y2Ba.我们首先研究了这些成分在皮质凝聚物中的存在。我们使用了三株标记F-actin(通过表达Lifeact::mKate2)的菌株以及内源性标记的N-WASP (sp -1::GFP)、capping蛋白(CAP-1::GFP)或Formin (CYK-1::GFP)。gydF4y2Ba23gydF4y2Ba.此外,我们使用了内源性标记ARP2/3复合物(ARX-2::mCherry)和N-WASP (wasp -1::GFP)的菌株。除了f -肌动蛋白,我们还鉴定出了wasp -1、ARP2/3复合物和帽蛋白CAP-124。gydF4y2Ba1 cgydF4y2Ba扩展数据图gydF4y2Ba1克ydF4y2Ba及补充影片gydF4y2Ba3.gydF4y2Ba而且gydF4y2Ba4gydF4y2Ba)为皮质凝聚物的组成部分,但Formin CYK-1缺失gydF4y2Ba19gydF4y2Ba,gydF4y2Ba24gydF4y2Ba(扩展数据图。gydF4y2Ba1克ydF4y2Ba).这表明,皮层凝聚物包含介导分支f -肌动蛋白成核的分子,例如,类似于CD44纳米簇、树突突触和模胞体gydF4y2Ba25gydF4y2Ba,gydF4y2Ba26gydF4y2Ba,gydF4y2Ba27gydF4y2Ba.我们还注意到,在他们大约10 s的生命周期(图。gydF4y2Ba1 fgydF4y2Ba)皮层凝聚物首先富集在wasp -1和ARP2/3中,然后才积累F-actin,然后先失去wasp -1和ARP2/3,然后失去F-actin(图。gydF4y2Ba1 d, egydF4y2Ba).考虑到它们出现的时间以及它们含有介导分支f -肌动蛋白成核的分子,我们推测动态皮层凝聚体在第一个卵母细胞皮层的形成中起着作用。gydF4y2Ba
我们接着问,皮质凝析液是否构成一种与周围环境共存的相。这种相以密集的材料特性(如密度)为特征,即与体积无关。我们使用同时标记F-actin和wasp -1的菌株来证明,在它们短暂的生命周期中(图2)。gydF4y2Ba1 e, fgydF4y2Ba),在Lifeact (gydF4y2Ba一个gydF4y2Ba)及wp -1 (gydF4y2BaWgydF4y2Ba)积分荧光强度(图;gydF4y2Ba1克gydF4y2Ba).我们通过分割确定的横截面积来估计皮质凝析液的体积gydF4y2Ba28gydF4y2Ba(gydF4y2Ba补充的方法gydF4y2Ba),并发现强度化学计量gydF4y2Ba\ (A / \左(A + W \) \)gydF4y2Ba在大约0.65到大约0.93之间,它们占据了一个体积gydF4y2BaVgydF4y2Ba通过计算f -肌动蛋白的体积贡献来很好地描述gydF4y2Ba\ ({v} _{一}\)gydF4y2Ba和WSP-1gydF4y2BaW W \ ({v} _ {} \)gydF4y2Ba,体积系数gydF4y2Ba\ ({v} _{一}= 1.54 \ *{10}^{7}\离开(\下午1 \ * {10}^ {8}\)\,{\ rm{\μ}}{{\ rm {m}}} ^ {3} \, {{\ rm {IU}}} ^ {1} \)gydF4y2Ba而且gydF4y2Ba\ ({v} _ {W}{10} = 2.34 \倍^{7}\离开(\下午2 \ * {10}^ {8}\)\,{\ rm{\μ}}{{\ rm {m}}} ^ {3} \, {{\ rm {IU}}} ^ {1} \)gydF4y2Ba(其中IU为总强度单位,见gydF4y2Ba方法gydF4y2Ba和无花果。gydF4y2Ba1我gydF4y2Ba).这提供了分子含量与体积之间的关系,但并不意味着凝析物是只有wasp -1和f -肌动蛋白密集排列的结构。而皮质凝析液在综合荧光强度上有两个数量级的变化(图。gydF4y2Ba1克gydF4y2Ba)时,皮层凝聚体中WSP-1和F-actin浓度的变化明显受到更大的限制(图。gydF4y2Ba1 hgydF4y2Ba).这也反映在f -肌动蛋白和WSP-1浓度的首选对的出现,由皮质凝聚物的集合维持平均(图。gydF4y2Ba1 jgydF4y2Ba).我们得出的结论是,一方面,皮质凝析液保持在远离平衡的状态:它们是高度动态的,每个在大约10秒后分解。另一方面,皮层凝聚物显示出多组分凝聚相的特征:它们占据由其分子含量决定的体积,并在不同于外部环境的浓度下显示出wp -1和f -肌动蛋白的富集gydF4y2Ba29gydF4y2Ba,gydF4y2Ba30.gydF4y2Ba.因此,随机出现、生长和随后溶解的皮质凝聚物的集合有效地形成了具有化学活性的微乳液,尽管不断翻转,但保持了稳定的尺寸分布,不会变粗gydF4y2Ba11gydF4y2Ba(无花果。gydF4y2Ba1 kgydF4y2Ba).缩合相的性质和其形成和溶解的机制都可以通过生长动力学的研究来揭示。gydF4y2Ba
皮质凝聚物生长规律gydF4y2Ba
为了研究这些皮层凝聚物的生长动力学,我们定量了它们的组成和体积随时间的变化(图。gydF4y2Ba2 gydF4y2Ba而且gydF4y2Ba补充的方法gydF4y2Ba).对于单个具有代表性的皮质凝聚物,图。gydF4y2Ba2 a, bgydF4y2Ba显示了(1)wp -1和F-actin总凝聚强度、(2)化学计量和(3)体积的时间演化(补充注释)gydF4y2Ba1克ydF4y2Ba而且gydF4y2Ba2 gydF4y2Ba).对于所示的例子,wp -1在生长和损失方面都领先于F-actin,化学计量量随时间单调增长,体积先增加后减少,并且通过将F-actin和wp -1的体积贡献相加可以很好地捕捉到。我们注意到,邻近的凝聚体在组成和体积上遵循相似的轨迹,尽管它们是在不同时间随机形成的(图2)。gydF4y2Ba1汉英gydF4y2Ba和扩展数据图。gydF4y2Ba9gydF4y2Ba).因此,在给定的时间,共享外部环境的相邻皮层凝聚体可能处于其内部生命周期的不同阶段。结果表明,凝析液的内部组成决定了凝析液成核后的生长动力学。gydF4y2Ba
一个gydF4y2Ba, wp -1::GFP(绿线)和Lifeact::mKate(品红线)的时间痕迹,来自代表性皮质凝析液的总凝析强度。gydF4y2BabgydF4y2Ba,时间痕迹的测量(实灰线)和确定(虚线灰)体积使用体积依赖于分子含量gydF4y2Ba\ ({v} _{一}+ {v} _ {W} W \)gydF4y2Ba和化学计量学gydF4y2Ba\ \(压裂{一}{+ W} \)gydF4y2Ba(黄线)为皮层凝聚物gydF4y2Ba一个gydF4y2Ba.蓝色阴影区域表示化学计量的范围,其中体积依赖性占测量体积(扩展数据图。gydF4y2Ba2 gydF4y2Ba).gydF4y2BacgydF4y2Ba,从9个卵母细胞的36930个凝析液的299165个时间点测量的质量通量相位肖像(实验,橙色和灰色箭头),并根据经验确定的生长规律计算(理论,黄色、绿色和蓝色箭头);参见扩展数据图。gydF4y2Ba10gydF4y2Ba对于单独的表示。颜色刻度表示时间速率变化矢量大小。粗线表示实验中的wasp -1(绿色)和F-actin(洋红色)零线;细线表示理论的零线。WSP-1的绝对分子量可以估计为8iu,大约相当于100个WSP-1分子。gydF4y2BadgydF4y2Ba,测量到的sp -1(绿色)和f -肌动蛋白(品红)生长速率作为化学计量量的函数显示出三种状态,分别为sp -1化学计量量零斜约0.85和f -肌动蛋白化学计量量零斜约0.9。gydF4y2BaegydF4y2Ba,gydF4y2BafgydF4y2Ba,相对wasp -1的线性依赖关系(gydF4y2BaegydF4y2Ba)和f -肌动蛋白(gydF4y2BafgydF4y2Ba)生长速率-在未受干扰的控制(蓝色)和温和gydF4y2Baarx-2gydF4y2BaRNAi(橙色)和中度RNAi(红色)案例-有效f -肌动蛋白体积分数gydF4y2BaϕgydF4y2Ba(gydF4y2Ba补充信息gydF4y2Ba).在蓝色阴影区域内保持线性(参见gydF4y2BabgydF4y2Ba扩展数据图gydF4y2Ba2 gydF4y2Ba),并用行表示,产生参数gydF4y2BakgydF4y2BargydF4y2Ba,gydF4y2BakgydF4y2BalgydF4y2Ba(gydF4y2BaegydF4y2Ba),gydF4y2BakgydF4y2BabgydF4y2Ba,gydF4y2BakgydF4y2BadgydF4y2Ba(gydF4y2BafgydF4y2Ba).gydF4y2BaggydF4y2Ba的结构下的反应母题gydF4y2BacgydF4y2Ba- - - - - -gydF4y2BafgydF4y2Ba由WSP-1自我募集、WSP-1依赖的f-肌动蛋白聚合、f-肌动蛋白依赖的WSP-1损失和f-肌动蛋白解聚组成。gydF4y2Ba
皮质凝聚物的内部成分如何影响其生长和收缩?为了回答这个问题,我们在分析凝析体的质量通量(质量平衡成像)的基础上,开发了一种定量研究多组分凝析体系综中成分动力学的通用方法gydF4y2Ba31gydF4y2Ba).为此,我们量化了皮层凝聚体中蛋白质数量的时间速率变化,作为其内部F-actin和wasp -1数量的函数。量的时间速率变化由一个向量场表示,它定义了wp -1和F-actin量空间中的平均轨迹(图2)。gydF4y2Ba2摄氏度gydF4y2Ba).与代表性实例一致(图;gydF4y2Ba2gydF4y2Ba),平均轨迹形成循环,通过三个后续机制:早期生长机制,其中冷凝物首先在wp -1中生长,随后在f -肌动蛋白中生长;WSP-1丢失而f -肌动蛋白数量仍在增加的过渡状态;以及同时失去WSP-1和F-actin的拆卸制度。wp -1动力学的零斜(图中的绿线)。gydF4y2Ba2摄氏度gydF4y2Ba),也就是说,凝析物含量高于其增长的wp -1量,低于其收缩的wp -1含量,反映了WSP-1增长依赖于f -肌动蛋白的临界wp -1量。在穿过原点的直线上,化学计量量是常数,因此sp -1零斜对应的阈值化学计量量约为0.85。f -肌动蛋白的生长动态变化从增长到收缩,其化学计量量相似,但略高,约为0.9(图中的洋红色线)。gydF4y2Ba2摄氏度gydF4y2Ba显示f -肌动蛋白零斜)。我们的结论是,在两个零斜之间的过渡状态下,皮质凝聚体变得不稳定,从生长到分解。gydF4y2Ba
这三种状态(生长,在wp -1零斜之上;过渡,两个零线之间的过渡;图中f -肌动蛋白零斜下方。gydF4y2Ba2摄氏度gydF4y2Ba)在绘制sp -1和F-actin生长速率作为化学计量学函数时也是可见的(图。gydF4y2Ba二维gydF4y2Ba).因为刻板的成分轨迹(图。gydF4y2Ba2 a, bgydF4y2Ba)化学计量量随时间单调增加,即gydF4y2BaxgydF4y2Ba图的轴。gydF4y2Ba二维gydF4y2Ba也表示时间的进展。生长速率对化学计量学的依赖揭示了sp -1和F-actin的相互调节,可以用图中所示的反应motif来描述。gydF4y2Ba2 ggydF4y2Ba.过程I和II由wasp -1介导,而过程III和IV由F-actin介导。过程I对应于wp -1的自我募集,在低化学计量时,对应于主要由wp -1组成的凝析油,wp -1的生长速度最大(图1)。gydF4y2Ba二维gydF4y2Ba).过程II表示依赖于wasp -1的f -肌动蛋白生长,反映为随着化学计量量的增加,f -肌动蛋白生长速率降低。这在图的过渡态中最为明显。gydF4y2Ba二维gydF4y2Ba.过程III表示sp -1的f -肌动蛋白依赖性损失,反映为sp -1的生长速率随着化学计量量的增加而降低。这表明f-肌动蛋白抵消了wasp -1自我招募的能力,类似于先前报道的f-肌动蛋白通过Rho对其成核的负反馈gydF4y2Ba15gydF4y2Ba,gydF4y2Ba32gydF4y2Ba.最后,过程IV表示f -肌动蛋白解聚,这反映在f -肌动蛋白在最高化学计量量时损失最快的事实(图4)。gydF4y2Ba二维gydF4y2Ba).对恒定的sp -1和F-actin数量下的sp -1和F-actin增长率的分析进一步支持了这一反应主题(扩展数据图)。gydF4y2Ba9gydF4y2Ba),以及分析参与调节F-actin的蛋白质的RNA干扰(RNAi)的影响(扩展数据图。gydF4y2Ba4gydF4y2Ba).gydF4y2Ba
被测相位肖像的形状(图;gydF4y2Ba2摄氏度gydF4y2Ba)和增长率的形状gydF4y2Ba\(\点{W} \)gydF4y2Ba适用于wp -1和gydF4y2Ba\({} \ \点)gydF4y2Ba为f -肌动蛋白作为化学计量学的函数(点表示时间导数;无花果。gydF4y2Ba二维gydF4y2Ba)提出了以下定义非线性动力系统的经验增长定律gydF4y2Ba33gydF4y2Ba(无花果。gydF4y2Ba2摄氏度gydF4y2Ba扩展数据图gydF4y2Ba3.gydF4y2Ba及补充说明gydF4y2Ba3.gydF4y2Ba):gydF4y2Ba
这里sp -1自我招募线性依赖于gydF4y2BaWgydF4y2Ba通过招聘率gydF4y2BakgydF4y2BargydF4y2Ba,与wasp -1分子二聚的能力相一致gydF4y2Ba34gydF4y2Ba,gydF4y2Ba35gydF4y2Ba(过程I). F-actin与wasp -1相互作用导致ARP2/3介导的分支成核,随后F-actin数量增加gydF4y2Ba36gydF4y2Ba,gydF4y2Ba37gydF4y2Ba.这种行为可以用术语来描述gydF4y2Ba\ ({k} _ {{\ rm {b}}} \压裂{AW} {V} \)gydF4y2Ba,在那里gydF4y2BakgydF4y2BabgydF4y2Ba动能系数是否描述了分支和冷凝体积gydF4y2Ba\ (V = {V} _{一}+ {V} _ {W} W \)gydF4y2Ba取决于分子数量(见上文及补充资料;过程II).分支形核与wasp -1中的损失同时发生;这种损失是由gydF4y2Ba\ ({k} _ {{\ rm {l}}} \压裂{AW} {V} \)gydF4y2Ba用动能系数gydF4y2BakgydF4y2BalgydF4y2Ba描述了sp -1的分支依赖损失(参考。gydF4y2Ba38gydF4y2Ba;最后,f -肌动蛋白随速率而损失gydF4y2BakgydF4y2BadgydF4y2Ba,与切断解聚一致gydF4y2Ba39gydF4y2Ba(过程IV)(也见扩展数据图中的简化描述。gydF4y2Ba6gydF4y2Ba).请注意,这四个系数一起捕捉了凝析油内部所有相关的分子过程。这可能包括上面没有讨论到的过程。这四项的数学形式是由观察到的相对增长率决定的gydF4y2Ba\ \点{W} / W \gydF4y2Ba而且gydF4y2Ba\ \(点{}/ \)gydF4y2Ba是有效f -肌动蛋白体积分数的线性函数gydF4y2Ba\ (\ varphi = \压裂{{v} _{一}}{v} \)gydF4y2Ba(无花果。gydF4y2Ba2 e, fgydF4y2Ba;另见补充说明中的讨论gydF4y2Ba3.gydF4y2Ba).数字gydF4y2Ba2 e, fgydF4y2Ba也允许我们进行估计gydF4y2BakgydF4y2BargydF4y2Ba,gydF4y2BakgydF4y2BalgydF4y2Ba,gydF4y2BakgydF4y2BabgydF4y2Ba而且gydF4y2BakgydF4y2BadgydF4y2Ba.有了这些估计,简单的增长定律很好地描述了实验数据,并捕获了整个质量通量相位肖像以及由零斜线反映的与成分相关的临界尺寸(图2)。gydF4y2Ba2摄氏度gydF4y2Ba).gydF4y2Ba
wp -1 nullclinegydF4y2Ba\ ({W} _ {{\ rm {c}}} (A) = A ({k} _ {{\ rm {l}}} - {k} _ {{\ rm {r}}} {v} _{一})/ {k} _ {{\ rm {r}}} {v} _ {W} \)gydF4y2Ba指定一个wp -1的临界量,超过这个临界量,wp -1的量就会增长,低于这个临界量,wp -1的量就会收缩。值得注意的是,这个临界量类似于成核和生长的临界液滴大小,但这里它源于生化反应,而不是凝结物理。所得到的生长规律在gydF4y2Ba\ \(左(W \右)= \左(0,0 \)\)gydF4y2Ba具有稳定(F-actin)和不稳定(wp -1)的方向。成核后,凝析液动力学遵循一个同斜轨道,最初在不稳定方向上快速增长,然后转向,最后在稳定方向上向固定点移动时发生解体。总之,这代表了凝聚态的动态不稳定性,与微管的动态不稳定性有相似之处gydF4y2Ba10gydF4y2Ba:皮层凝聚体由不稳定增长过渡到收缩,这限制了其大小,并可以显示随机救援事件(扩展数据图。gydF4y2Ba7gydF4y2Ba).gydF4y2Ba
向无限制增长过渡gydF4y2Ba
为了了解凝析液生长到凝析液分解的转变是如何安排的,我们使用RNAi扰乱了wasp -1和F-actin之间的相互作用。调控f -肌动蛋白组装的上游信号分子的RNAi,如Rho -1 (Rho GTPase), CYK-1, CDC-42和CHIN-1 (CDC-42 GAP),以及多价接头VAB-1 (Ephrin受体)和Nck -1 (Nck)不影响凝析动力学gydF4y2Ba40gydF4y2Ba,gydF4y2Ba41gydF4y2Ba,gydF4y2Ba42gydF4y2Ba(扩展数据图。gydF4y2Ba4gydF4y2Ba及补充说明gydF4y2Ba4gydF4y2Ba而且gydF4y2Ba7gydF4y2Ba).这表明皮层凝聚动力学是由独立于调节肌动球蛋白皮层的主要信号通路的反馈结构控制的gydF4y2Ba43gydF4y2Ba.wasp -1通过ARP2/3复合物介导f -肌动蛋白的分支成核gydF4y2Ba4gydF4y2Ba,gydF4y2Ba35gydF4y2Ba,因此我们对ARX-2 (ARP2 /3复合物中的ARP2)进行了RNAigydF4y2Ba秀丽隐杆线虫gydF4y2Ba44gydF4y2Ba).卵母细胞的皮质凝析物数量减少少于20小时gydF4y2Baarx-2gydF4y2BaRNAi,而皮质凝聚物在超过20小时的RNAi中不存在(图。gydF4y2Ba3 a, bgydF4y2Ba和扩展数据图。gydF4y2Ba7一个gydF4y2Ba),与f -肌动蛋白分支形核的普遍减少相一致gydF4y2Ba45gydF4y2Ba.gydF4y2Ba
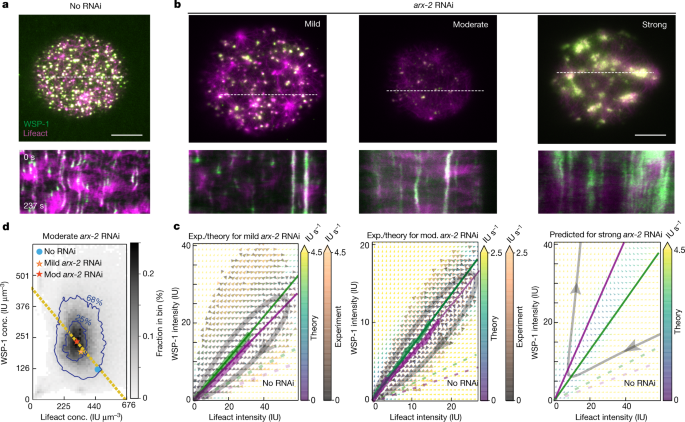
一个gydF4y2Ba,上,未受干扰的对照卵母细胞皮层凝聚物的TIRF图像。底部,kymograph(沿白色虚线确定)显示时间动态。gydF4y2BabgydF4y2Ba,上,轻、中、重度皮质凝聚物的TIRF图像gydF4y2Baarx-2gydF4y2BaRNAi(从左到右)。轻度和中度gydF4y2Baarx-2gydF4y2BaRNAi数据集名义上对应于18-20和19-20小时gydF4y2Baarx-2gydF4y2Ba分别为RNAi,并在稳态(gydF4y2Ba补充信息gydF4y2Ba).底部,各自的轨迹图(由白色虚线确定)揭示了时间动态。比例尺,10 μm (gydF4y2Ba一个gydF4y2Ba,gydF4y2BabgydF4y2Ba).gydF4y2BacgydF4y2Ba,实验(经验,橙色和灰色箭头)和理论(理论,黄色,绿色和蓝色箭头)轻度和中度质量通量相位肖像gydF4y2Baarx-2gydF4y2BaRNAi卵母细胞(左和中间),预测严重gydF4y2Baarx-2gydF4y2BaRNAi相位图(右)使用gydF4y2BakgydF4y2BadgydF4y2Ba估计从渐进式变化gydF4y2BakgydF4y2BadgydF4y2Ba从对照到适度RNAi数据集(扩展数据图。gydF4y2Ba7gydF4y2Ba及补充说明)。颜色表示时间速率变化矢量大小。粗线表示测量到的wasp -1(洋红色)和f -肌动蛋白(绿色)零线;细线表示理论的零线。虚线表示未受干扰的对照卵母细胞的空斜(图。gydF4y2Ba2摄氏度gydF4y2Ba;扩展数据图。gydF4y2Ba10 bgydF4y2Ba在单个图中显示空线)。代表性的流线用灰色表示。gydF4y2BadgydF4y2Ba,凝析液中f -肌动蛋白和wasp -1瞬时浓度的直方图gydF4y2Baarx-2gydF4y2BaRNAi。这里68%和25%的瞬时凝析液浓度落在各自的蓝色等高线内。蓝色圆点和橙色和红色星点代表了轻度和中度对照的优先维持浓度对gydF4y2Baarx-2gydF4y2Ba分别为RNAi卵母细胞。黄色虚线:由体积关系给出的总密度恒定线。gydF4y2Ba
我们使用皮质凝析液数量的减少作为扰动强度的衡量标准,并将其分为轻度(每个卵母细胞30 ~ 70个凝析液)、中度(每个卵母细胞70 ~ 120个凝析液)和强扰动gydF4y2Baarx-2gydF4y2BaRNAi(无动态皮质凝聚物)。轻度和中度情况下皮质凝聚物的质量平衡成像显示,与未受干扰的情况相比,成分轨迹逐渐向wasp -1轴倾斜(图2)。gydF4y2Ba3 cgydF4y2Ba).生长规律的数学形式保持不变,但相关系数发生了变化(图2)。gydF4y2Ba2 e, fgydF4y2Ba).轻度和中度gydF4y2Baarx-2gydF4y2BaRNAi降低了wasp -1的自我募集率gydF4y2BakgydF4y2BargydF4y2Ba分别提高了17±4%和15±4%,增大了系数gydF4y2BakgydF4y2BalgydF4y2Ba对温和的gydF4y2Baarx-2gydF4y2BaRNAi降低20±6%(1±5%)。分支系数gydF4y2BakgydF4y2BabgydF4y2Ba保持基本不变,表明ARP2/3的数量并不是ARP2/3介导的皮层凝聚体内分支的速率限制。效果以轻度和中度为主gydF4y2Baarx-2gydF4y2BaRNAi分别是f -肌动蛋白损失率的1.7倍和2.7倍gydF4y2BakgydF4y2BadgydF4y2Ba.这与之前的研究结果一致,ARP2/3复合物在体外保护f -肌动蛋白免于解聚gydF4y2Ba46gydF4y2Ba.除系数变化外,有轻度和中度之分gydF4y2Baarx-2gydF4y2BaRNAi分别将平均F-actin浓度降低了约1.4和1.5倍,并将平均wp -1浓度分别提高了约1.5和1.8倍(图2)。gydF4y2Ba3 dgydF4y2Ba).三种情况均无RNAi对照,分为轻度和中度gydF4y2Baarx-2gydF4y2BaRNAi,平均浓度对一起落在sp -1和F-actin总密度不变的直线上(图。gydF4y2Ba3 dgydF4y2Ba,黄色虚线;看到gydF4y2Ba补充信息gydF4y2Ba).我们得出结论,ARP2/3配合物主要通过其对f -肌动蛋白分解的影响,控制着从凝析液增长到凝析液分解的转变,并决定了沿总密度恒定线的内部浓度的整体平均对。gydF4y2Ba
RNAi对ARX-2的强烈消耗(在20°C下RNAi喂养超过20小时)导致动态皮质凝析物的损失,并导致皮质结构显著改变,出现大面积的F-actin和wp -1斑块(图2)。gydF4y2Ba3 bgydF4y2Ba,对,补充视频gydF4y2Ba5gydF4y2Ba和扩展数据图。gydF4y2Ba8gydF4y2Ba).我们想知道,根据上面的凝析液生长规律,是否可以理解这种表型。这是不可能确定的四个增长规律系数强gydF4y2Baarx-2gydF4y2BaRNAi采用质量平衡成像,因为没有动态凝聚物。但是,系统变化的同时f -肌动蛋白的损失率gydF4y2BakgydF4y2BadgydF4y2Ba以及每个卵母细胞凝聚数的增加gydF4y2Baarx-2gydF4y2BaRNAi使我们能够提供一个下限估计gydF4y2BakgydF4y2BadgydF4y2Ba为强RNAi条件(扩展数据图。gydF4y2Ba7gydF4y2Ba).我们发现,在这个估计值及以上gydF4y2BakgydF4y2BadgydF4y2Ba系统会越过一个临界点,在这个临界点上,两个零斜切换了它们的位置,此时f -肌动蛋白零斜高于wasp -1零斜(图1)。gydF4y2Ba3 cgydF4y2Ba,对吧)。这导致皮质凝聚体的生长动力学发生显著变化,从生长到收缩的同斜轨道完全丧失。相反,凝析液表现出无界生长,与大面积持久的f -肌动蛋白和wasp -1斑块的出现一致(图2)。gydF4y2Ba3 bgydF4y2Ba,对吧;请注意,我们预计无限的增长最终会受到我们在描述中没有考虑到的影响的限制,例如单体池的耗尽)。总之,我们的分析表明,零斜位置的转换在强gydF4y2Baarx-2gydF4y2BaRNAi导致不受控制的f -肌动蛋白生长和受损的卵母细胞皮层激活,因此受损的后期发育gydF4y2Ba22gydF4y2Ba,gydF4y2Ba47gydF4y2Ba(补充笔记gydF4y2Ba5gydF4y2Ba而且gydF4y2Ba6gydF4y2Ba).gydF4y2Ba
套装属性gydF4y2Ba
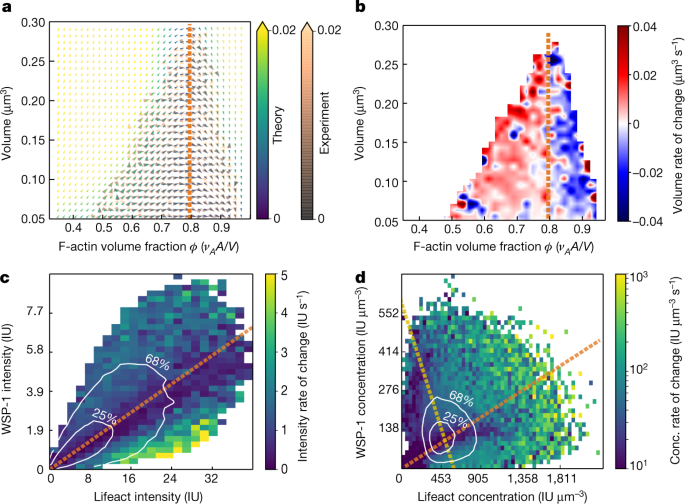
生长动力学如何导致特定的内部平均浓度对,从而特定的化学计量?为了解决这个问题,我们改变了f -肌动蛋白量的变量gydF4y2Ba一个gydF4y2Ba和wp -1量gydF4y2BaWgydF4y2Ba到有效f -肌动蛋白体积分数gydF4y2Ba\ (\ varphi = {v} _{一}/ v \)gydF4y2Ba冷凝液体积gydF4y2BaVgydF4y2Ba.数字gydF4y2Ba4gydF4y2Ba所计算的相位肖像gydF4y2Ba\ \ varphi \ ()gydF4y2Ba- - - - - -gydF4y2Ba\ \ (V)gydF4y2Ba将经验确定的生长规律进行变量变换得到的平面与实测的wp -1、F-actin量和凝析液体积确定的实验平面相一致。数字gydF4y2Ba4 bgydF4y2Ba显示从凝析物增长(红色)到收缩(蓝色)的转变发生在有效f -肌动蛋白体积分数约为0.8时,对应的化学计量量约为0.86。值得注意的是,在这个化学计量中,凝析液体积和化学计量的变化率是最慢的(图中的橙色虚线)。gydF4y2Ba4 a, b, dgydF4y2Ba),这意味着动态凝聚体的集合是由这种缓慢变化的,因此占主导地位的化学计量学所控制的。因此,浓度直方图的峰值(图。gydF4y2Ba1 jgydF4y2Ba而且gydF4y2Ba3 dgydF4y2Ba)发生在主要化学计量线与恒定总密度线相交的点(图2)。gydF4y2Ba4 dgydF4y2Ba).gydF4y2Ba
一个gydF4y2Ba,冷凝液动力学的相肖像gydF4y2Ba\ \ varphi \ ()gydF4y2Ba- - - - - -gydF4y2Ba\ \ (V)gydF4y2Ba飞机。橙色和灰色箭头由测量到的wp -1和f -肌动蛋白量确定,与图中相反。gydF4y2Ba2摄氏度gydF4y2Ba,基于皮质凝析液具有球形的假设,使用测量的凝析液体积。黄色、绿色和蓝色箭头是根据经验确定的增长规律计算出来的gydF4y2Ba\ \ varphi \ ()gydF4y2Ba- - - - - -gydF4y2Ba\ \ (V)gydF4y2Ba飞机。颜色表示时间速率变化矢量大小。粗线表示实验确定的体积零斜。gydF4y2BabgydF4y2Ba,体积变化率作为瞬时体积和有效f -肌动蛋白体积分数的函数。凝析液在有效f -肌动蛋白体积分数为0.8(橙色虚线)时从增长过渡到收缩,这对应于过渡区域内动力学缓慢的区域(图2)。gydF4y2Ba二维gydF4y2Ba而且gydF4y2BacgydF4y2Ba而且gydF4y2BadgydF4y2Ba).gydF4y2BacgydF4y2Ba,质量通量相像电流大小。等高线(68%,25%)描述了最常用的总强度值。橙色虚线表示转换区域中心对应的有效f -肌动蛋白体积分数(图2)。gydF4y2Ba二维gydF4y2Ba),并与最低总电流和最慢动力学相吻合。gydF4y2BadgydF4y2Ba,浓度磁通相像电流大小。等高线(68%,25%)描述了最常用的浓度值,反映了一对浓度的优先维持。这对浓度位于总密度恒定线(黄色)和主要化学计量线(橙色)的交叉点,这对应于中的橙色线gydF4y2Ba一个gydF4y2Ba- - - - - -gydF4y2BacgydF4y2Ba和图的过渡区域。gydF4y2Ba2 c, dgydF4y2Ba(参见扩展数据图。gydF4y2Ba5gydF4y2Ba对温和的gydF4y2Baarx-2gydF4y2BaRNAi条件)。gydF4y2Ba
强烈的化学反应动力学gydF4y2Ba
我们还认识到有效f -肌动蛋白体积分数的时间演化gydF4y2Ba\ ({\ varphi} \ \点)gydF4y2Basp -1和F-actin浓度与凝析液体积无关(补充说明)gydF4y2Ba8gydF4y2Ba- - - - - -gydF4y2Ba10gydF4y2Ba).因此,凝聚态动力学是密集的,这与混合体系中的质量作用动力学是一致的。然而,传统的质量作用动力学在恒定体积下改变反应物的浓度,但通常不涉及组装和拆卸,就像这里的情况一样。值得注意的是,密集凝析油动力学与传统的类液体凝析油成核和生长动力学并不一致,在这种动力学中,凝析油的组装速率取决于凝析油的大小gydF4y2Ba48gydF4y2Ba,gydF4y2Ba49gydF4y2Ba.这表明,皮层凝聚体表现出一种非常规的化学动力学,在这种动力学中,质量作用支配着凝聚体的组装和拆卸,因此质量作用动力学对凝聚体浓度的影响被修正了(补充注释)gydF4y2Ba8gydF4y2Ba- - - - - -gydF4y2Ba10gydF4y2Ba).然而,需要注意的是,即使皮质凝聚体不通过经典的成核和生长组装,密集的凝聚体动力学表明,凝聚体材料表现为具有尺寸无关特性的混合良好的相。当凝聚体扩散的时间短于与化学反应相关的典型时间时,预计会出现强烈的反应动力学。凝聚体动态不稳定性限制了皮层凝聚体的大小。因此,反应动力学仍然强烈,所生成的化学活性微乳液保持稳定状态的尺寸分布(图2)。gydF4y2Ba1 kgydF4y2Ba)gydF4y2Ba11gydF4y2Ba.gydF4y2Ba
讨论gydF4y2Ba
综上所述,皮质凝聚体是一种新型的非平衡生物分子凝聚体,其组装和拆卸是由质量作用化学动力学控制的非线性动态过程。它们招募分子,驱动f -肌动蛋白的分支成核,并支持肌动球蛋白皮层的激活。皮质凝聚体的生长和收缩动力学与微管生长和收缩的动态不稳定性相似gydF4y2Ba10gydF4y2Ba,但在形成相的散装组件中出现。我们认为,皮层凝聚体的形成和随后通过凝聚体动态不稳定性的溶解,有助于控制自催化f -肌动蛋白成核,并防止大脑中第一个皮层肌动蛋白网激活期间的失控增长gydF4y2Ba秀丽隐杆线虫gydF4y2Ba卵母细胞。gydF4y2Ba
方法gydF4y2Ba
看到gydF4y2Ba补充的方法gydF4y2Ba.gydF4y2Ba
报告总结gydF4y2Ba
有关研究设计的进一步资料,请参阅gydF4y2Ba自然研究报告摘要gydF4y2Ba链接到这篇文章。gydF4y2Ba
数据可用性gydF4y2Ba
凝析油跟踪数据可在gydF4y2Bahttps://doi.org/10.17617/3.PIRFA2gydF4y2Ba.gydF4y2Ba源数据gydF4y2Ba提供了这篇论文。gydF4y2Ba
代码的可用性gydF4y2Ba
自定义代码可在gydF4y2Bahttps://doi.org/10.17617/3.PIRFA2gydF4y2Ba.gydF4y2Ba
参考文献gydF4y2Ba
Salbreux, G., Charras, G. & Paluch, E.肌动蛋白皮层力学和细胞形态发生。gydF4y2Ba细胞生物学趋势。gydF4y2Ba22gydF4y2Ba, 536-545(2012)。gydF4y2Ba
拉森,s.m.等人。哺乳动物卵母细胞的皮质力学和减数分裂II完成是由肌球蛋白II和Ezrin-Radixin-Moesin (ERM)蛋白介导的。gydF4y2Ba摩尔。杂志。细胞gydF4y2Ba21gydF4y2Ba, 3182-3192(2010)。gydF4y2Ba
李,李,李,李。小鼠卵母细胞成熟过程中对称性破缺与极性建立。gydF4y2Ba费罗斯。反式。r . Soc。Lond。B杂志。科学。gydF4y2Ba368gydF4y2Ba, 20130002(2013)。gydF4y2Ba
波拉德,T. D. &库珀,J. A.肌动蛋白和肌动蛋白结合蛋白。对机制和功能的批判性评价。gydF4y2Ba为基础。学生物化学启。gydF4y2Ba55gydF4y2Ba, 987-1035(1986)。gydF4y2Ba
Su, x等。信号分子的相分离促进T细胞受体信号转导。gydF4y2Ba科学gydF4y2Ba352gydF4y2Ba, 595-599(2016)。gydF4y2Ba
Kim, S, Kalappurakkal, J. M. Mayor, S. & Rosen, M. K.肾素磷酸化诱导通过肌动球蛋白收缩移动的相分离结构域。gydF4y2Ba摩尔。杂志。细胞gydF4y2Ba30.gydF4y2Ba, 2996-3012(2019)。gydF4y2Ba
张晓明,张晓明,张晓明。肌动蛋白信号蛋白相分离簇活性的化学计量学控制。gydF4y2Ba科学gydF4y2Ba363gydF4y2Ba, 1093-1097(2019)。gydF4y2Ba
威里奇,K., Dasbiswas, K., Witten, T., Vaikuntanathan, S. & Gardell, M.自组织电机分离活性液滴。gydF4y2Ba国家科学院学报美国gydF4y2Ba116gydF4y2Ba, 11125-11130(2019)。gydF4y2Ba
海曼,A. A.,韦伯,C. A. & Jülicher, F.生物学中的液-液相分离。gydF4y2Ba为基础。细胞发育生物学。gydF4y2Ba30.gydF4y2Ba, 39-58(2014)。gydF4y2Ba
米契森,T. & Kirschner .微管生长的动态不稳定性。gydF4y2Ba自然gydF4y2Ba312gydF4y2Ba, 237-242(1984)。gydF4y2Ba
Zwicker, D. Hyman, A. A. & Jülicher, F.活性乳剂中奥斯特瓦尔德成熟的抑制。gydF4y2Ba理论物理。启EgydF4y2Ba92gydF4y2Ba, 012317(2015)。gydF4y2Ba
Santella, L., Limatola, N. & Chun, J. T.卵母细胞成熟和受精的细胞和分子方面:从肌动蛋白细胞骨架的角度。gydF4y2Ba动物。gydF4y2Ba6gydF4y2Ba, 5(2020)。gydF4y2Ba
布鲁内,S.和Verlhac, m.h.摆脱减数分裂的定位:分裂的不对称性。gydF4y2Ba嗡嗡声。天线转换开关。更新gydF4y2Ba17gydF4y2Ba, 68-75(2011)。gydF4y2Ba
施罗德,T. E. & Stricker, S. A.海星卵母细胞成熟过程中的形态变化:表面超微结构和皮层肌动蛋白。gydF4y2BaDev,杂志。gydF4y2Ba98gydF4y2Ba, 373-384(1983)。gydF4y2Ba
Bement, W. M.等。Rho信号和肌动蛋白组装之间的激活剂-抑制剂偶联使细胞皮层成为可兴奋的介质。gydF4y2Ba细胞生物学。gydF4y2Ba17gydF4y2Ba, 1471-1483(2015)。gydF4y2Ba
卵母细胞减数分裂成熟和受精的控制。gydF4y2BaWormBookgydF4y2Bahttps://doi.org/10.1895/wormbook.1.53.1gydF4y2Ba(2005)。gydF4y2Ba
维拉德,N, Gunsalus, K. C. & Piano, F.肌动蛋白的不同作用gydF4y2Ba秀丽隐杆线虫gydF4y2Ba早期胚胎发生。gydF4y2BaBMC发展生物学。gydF4y2Ba7gydF4y2Ba, 142(2007)。gydF4y2Ba
哈里斯,J. E.等。主要精子蛋白信号通路促进受精前卵母细胞微管重组gydF4y2Ba秀丽隐杆线虫gydF4y2Ba.gydF4y2BaDev,杂志。gydF4y2Ba299gydF4y2Ba, 105-121(2006)。gydF4y2Ba
斯旺,K. A.等。Cyk-1:gydF4y2Ba秀丽隐杆线虫gydF4y2Ba胚胎细胞质分裂后期需要FH基因。gydF4y2Ba细胞科学。gydF4y2Ba111gydF4y2Ba, 2017-2027(1998)。gydF4y2Ba
赖希,j.d.等人。PAR极性网络的调节激活确保了对空间线索的及时和具体的反应。gydF4y2Ba咕咕叫。医学杂志。gydF4y2Ba29gydF4y2Ba, 1911 - 1923。e5(2019)。gydF4y2Ba
Funatsu, T., Harada, Y., Tokunaga, M., Saito, K. & Yanagida, T.水溶液中单个肌凝蛋白分子对单个荧光分子和单个ATP翻转的成像。gydF4y2Ba自然gydF4y2Ba374gydF4y2Ba, 555-559(1995)。gydF4y2Ba
Severson, a.f, Baillie, D. L. & Bowerman, B. formin同源蛋白和profilin是细胞分裂和arp2 /3独立的皮质微丝组装所必需的gydF4y2Ba秀丽隐杆线虫gydF4y2Ba.gydF4y2Ba咕咕叫。医学杂志。gydF4y2Ba12gydF4y2Ba, 2066-2075(2002)。gydF4y2Ba
朱,Z.等。WAVE和WASP的功能协调gydF4y2Ba秀丽隐杆线虫gydF4y2Ba成神经细胞迁移。gydF4y2BaDev细胞。gydF4y2Ba39gydF4y2Ba, 224-238(2016)。gydF4y2Ba
billault - chaummartin, I. & Martin, S. G. Capping蛋白使arp2 /3-组装的肌动蛋白斑块与formins绝缘。gydF4y2Ba咕咕叫。医学杂志。gydF4y2Ba29gydF4y2Ba, 3165 - 3176。e6(2019)。gydF4y2Ba
Sil, P.等。动态肌动蛋白介导的CD44纳米级聚类调节其在质膜上的中尺度组织。gydF4y2Ba摩尔。杂志。细胞gydF4y2Ba31gydF4y2Ba, 561-579(2020)。gydF4y2Ba
韦格纳,a.m.等人。N-wasp和arp2/3复合物是肌动蛋白在树突棘和突触发育中的关键调节因子。gydF4y2Ba生物。化学。gydF4y2Ba283gydF4y2Ba, 15912-15920(2008)。gydF4y2Ba
Murphy, D. A. & Courtneidge, S. A.模胞体和非模胞体的“进”和“出”:特征、形成和功能。gydF4y2Ba细胞生物学。gydF4y2Ba12gydF4y2Ba, 413-426(2011)。gydF4y2Ba
伯格,S.等人。Ilastik:交互式机器学习(生物)图像分析。gydF4y2BaNat方法。gydF4y2Ba16gydF4y2Ba, 1226-1232(2019)。gydF4y2Ba
瑞巴克,J. A. & Brangwynne, C. P.相分离能否缓冲细胞噪声?gydF4y2Ba科学gydF4y2Ba367gydF4y2Ba, 364-365(2020)。gydF4y2Ba
混合物热力学(多组分系统)。gydF4y2Ba化学。Thermodynam。gydF4y2Bahttps://doi.org/10.1007/978-3-642-19864-9_6gydF4y2Ba(2012)。gydF4y2Ba
西川,M., Naganathan, s.r., Jülicher, F. & Grill, s.w.控制肌动球蛋白皮质的收缩不稳定性。gydF4y2BaeLifegydF4y2Ba6gydF4y2Ba, e19595(2017)。gydF4y2Ba
王欣,葛蕾塔,B. Cooper, J. & Carlsson, A.内吞作用中的肌动蛋白调节反馈作用。gydF4y2BaBiophys。J。gydF4y2Ba110gydF4y2Ba, 1430-1443(2016)。gydF4y2Ba
施特罗加茨,s.h.。gydF4y2Ba非线性动力学和混沌:与应用到物理学,生物学,化学和工程gydF4y2Ba(西景出版社,2014)。gydF4y2Ba
潘立克,S. B. & Rosen, M. K. WASP家族蛋白信号整合的物理机制。gydF4y2Ba为基础。学生物化学启。gydF4y2Ba79gydF4y2Ba, 707-735(2010)。gydF4y2Ba
Arp2/3复合物和formmins对肌动蛋白丝组装的调控。gydF4y2Ba为基础。启Biophys。Biomol。结构体。gydF4y2Ba36gydF4y2Ba, 451-477(2007)。gydF4y2Ba
马昌德,J. B.,凯撒,D. A.,波拉德,T. D.和希格斯,H. N. WASP/Scar蛋白与肌动蛋白和脊椎动物Arp2/3复合物的相互作用。gydF4y2Ba细胞生物学。gydF4y2Ba3.gydF4y2Ba, 76-82(2001)。gydF4y2Ba
Dürre, K.等。蛋白控制的肌动蛋白聚合形成脂膜。gydF4y2BaCommun Nat。gydF4y2Ba9gydF4y2Ba, 1630(2018)。gydF4y2Ba
史密斯,b.a.等人。三色单分子成像显示WASP脱离Arp2/3复合物触发肌动蛋白丝分支形成。gydF4y2BaeLifegydF4y2Ba2 gydF4y2Ba, e01008(2013)。gydF4y2Ba
肌动蛋白丝的解聚和切断机制及其在细胞骨架动力学中的意义。gydF4y2BaInt。启Cytol。gydF4y2Ba258gydF4y2Ba, 1-82(2007)。gydF4y2Ba
Rho GTPases和肌动蛋白细胞骨架。gydF4y2Ba科学gydF4y2Ba279gydF4y2Ba, 509-514(1998)。gydF4y2Ba
George, S. E, Simokat, K., Hardin, J. & Chisholm, A. D. VAB-1 Eph受体酪氨酸激酶在神经和上皮形态发生中的功能gydF4y2Ba秀丽隐杆线虫gydF4y2Ba.gydF4y2Ba细胞gydF4y2Ba92gydF4y2Ba, 633-643(1998)。gydF4y2Ba
Mohamed, a.m. & Chin-Sang, i.d. ThegydF4y2Ba秀丽隐杆线虫gydF4y2BaNck-1基因编码两种亚型,是神经元引导所必需的。gydF4y2BaDev,杂志。gydF4y2Ba354gydF4y2Ba, 55-66(2011)。gydF4y2Ba
戴维斯等人。高分辨率时间分析揭示了细胞质分裂分子调节的功能时间轴。gydF4y2BaDev细胞。gydF4y2Ba30.gydF4y2Ba, 209-223(2014)。gydF4y2Ba
Sawa, M.等。的重要角色gydF4y2Ba秀丽隐杆线虫gydF4y2BaArp2/3复合物在腹壳细胞迁移中的作用。gydF4y2Ba细胞科学。gydF4y2Ba116gydF4y2Ba, 1505-1518(2003)。gydF4y2Ba
Roh-Johnson, M. & Goldstein, B. Arp2/3在皮质肌动蛋白组织中的体内作用gydF4y2Ba秀丽隐杆线虫gydF4y2Ba原肠胚形成。gydF4y2Ba细胞科学。gydF4y2Ba122gydF4y2Ba, 3983-3993(2009)。gydF4y2Ba
Mullins, R. D. Heuser, J. A. & Pollard, T. D. Arp2/3复合物与肌动蛋白的相互作用:成核、高亲和力尖端旋盖和细丝分支网络的形成。gydF4y2Ba国家科学院学报美国gydF4y2Ba95gydF4y2Ba, 6181-6186(1998)。gydF4y2Ba
Naganathan, S. R.等。肌动球蛋白皮质的形态发生退化。gydF4y2BaeLifegydF4y2Ba7gydF4y2Ba, e37677(2018)。gydF4y2Ba
韦伯,C. A., Zwicker, D., Jülicher, F. & Lee, C. F.活性乳剂的物理。gydF4y2Ba众议员掠夺。理论物理。gydF4y2Ba82gydF4y2Ba, 064601(2019)。gydF4y2Ba
Kashchiev D。gydF4y2Ba成核:基础理论与应用gydF4y2Ba(Butterworth-Heinemann, 2000)。gydF4y2Ba
确认gydF4y2Ba
S.W.G.得到了DFG(授权号TRR 83, GR 3271/2, GR 3271/3和GR 3271/4)和欧洲研究理事会(授权号742712和h2020 - mca - itn -2015)的支持。V.T.Y.承认玛丽·斯科佐多夫斯卡-居里行动(批准不。H2020-MSCA-ITN-2015)。A.N.感谢MPI-PKS和MPI-CBG的ELBE项目的资助和支持。这项工作由马克斯·普朗克学会资助,并在德国卓越战略no. 1下得到DFG的支持。exc - 2068 - 390729961。我们非常感谢2017年和2019年MBL生理学课程的教职员工和学生,特别是A. Chakrabarti, M. Dietrich, G. Martinez, M. Mirvis和Q. Yu。我们感谢A. Bhatnagar, S. Choubey, K. Crell, E. Garner, J. Geisler, N. Goehring, M. Holmes, A. Honigman, T. Middlekoop, A. Mukherjee, J. Reich和G. Squyres的实验帮助和讨论。我们感谢J. Brugués, O. Campàs, P. Gönczy和W. Grill对手稿的批评意见。gydF4y2Ba
资金gydF4y2Ba
马克斯·普朗克学会提供的开放获取资金。gydF4y2Ba
作者信息gydF4y2Ba
作者及隶属关系gydF4y2Ba
贡献gydF4y2Ba
V.T.Y, a.n., F.J.和S.W.G.设计了这项研究。v.t.y和A.N.完成了所有的实验。A.N.和V.T.Y.在S.W.G.的指导下进行了分析,F.J. T.W.提供了实验支持,并产生了组成性不活跃的NCK-1菌株。a.n., V.T.Y, F.J.和S.W.G.发展了理论并撰写了手稿。gydF4y2Ba
相应的作者gydF4y2Ba
道德声明gydF4y2Ba
相互竞争的利益gydF4y2Ba
作者声明没有利益竞争。gydF4y2Ba
同行评审gydF4y2Ba
同行评审信息gydF4y2Ba
自然gydF4y2Ba感谢Andreas Bausch, Jonathon Ditlev, Martin Lenz和其他匿名审稿人对本工作的同行评审所做的贡献。gydF4y2Ba
额外的信息gydF4y2Ba
出版商的注意gydF4y2Ba施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。gydF4y2Ba
扩展的数据图形和表格gydF4y2Ba
扩展数据图1皮质凝析液组分。gydF4y2Ba
一个gydF4y2Ba, Top, eGFP三色成像::WSP1;ARX2::tagRFP和LifeAct::HaloTag;放大的插图和底部显示了一个具有代表性的皮质凝聚例子(盒装)及其时间演变,揭示了成分到达的顺序是sp -1,其次是ARX-2和F-actin。gydF4y2BaBgydF4y2Ba, Top, CAP-1双色成像::eGFP;Life-Act::mkate2,放大的插图和底部显示了一个具有代表性的皮层凝聚例子(盒装)及其时间演变,揭示了CAP-1在F-actin之后。gydF4y2BaCgydF4y2Ba,比较各组件的时间顺序gydF4y2Ba一个gydF4y2Ba,gydF4y2BaBgydF4y2Ba通过对最大LifeAct信号的时间比对,发现各组分募集的顺序为sp -1、ARP2/3、F-actin和CAP-1。gydF4y2BaDgydF4y2Ba, Top, CAP-1双色成像::eGFP;LifeAct::mkate2,放大的插图和底部显示了一个具有代表性的皮质凝聚示例(盒装)及其时间演变。CYK-1/Formin不存在于皮质凝聚物中,但在大规模收缩前的收缩肌动球蛋白脉冲中发现。gydF4y2BaEgydF4y2Ba,通过Utrophin标记f -肌动蛋白(左)导致的时间序列与通过LifeAct标记f -肌动蛋白(右)相似。底部图像,各自的kymograph确定沿虚线白。请注意,在LifeAct和Utrophin都被成像的情况下(右),由于差异漂白,前几帧的两个通道之间的共定位很高。比例尺,10µm。gydF4y2Ba
图2分子含量与体积的关系。gydF4y2Ba
当F-actin体积分数φ <~ 0.6和φ >~ 0.9时,测量体积与wp -1和F-actin强度线性组合的偏差。注意图中与线性的偏差。gydF4y2Ba2 e, fgydF4y2Ba与体积分数偏离V = V的范围相吻合gydF4y2Ba一个gydF4y2BaA + vgydF4y2BaWgydF4y2BaW。gydF4y2Ba
图3质量通量相位图切片证实了经验增长规律。gydF4y2Ba
一个gydF4y2Ba,gydF4y2BaBgydF4y2Ba, wp -1 (gydF4y2Ba一个gydF4y2Ba)和f -肌动蛋白(gydF4y2BaBgydF4y2Ba)在恒定的LifeAct水平下,作为wp -1函数的生长速率(圆点颜色暗度的增加表示图中第一、第二和第三个最低的LifeAct箱。gydF4y2Ba2摄氏度gydF4y2Ba分别)。gydF4y2BaCgydF4y2Ba,gydF4y2BaDgydF4y2Ba, wp -1 (gydF4y2BaCgydF4y2Ba)和f -肌动蛋白(gydF4y2BaDgydF4y2Ba)在恒定的wp -1水平下,生长速率作为f -肌动蛋白的函数(圆点颜色暗度的增加表示图中wp -1最低的第一、第二和第三个箱。gydF4y2Ba2摄氏度gydF4y2Ba分别)。Insets的gydF4y2Ba模拟gydF4y2Ba表示有贡献的反馈过程(图;gydF4y2Ba2 ggydF4y2Ba).gydF4y2Ba
图4皮层凝聚体的RNAi扰动。gydF4y2Ba
a -gydF4y2Ba,左边两幅图,通过荧光成像量化24小时RNAi的疗效(右)和相对于非RNAi对照的蛋白质水平的相对变化(左)。右侧两个面板,非RNAi对照组(左)和RNAi 24小时后(右)皮层凝聚物的wp -1和LifeAct荧光图像,以及沿着白线确定的各自的kymographs(下)。gydF4y2Ba模拟gydF4y2Ba对ARX-2、UNC-60、CAP-1或COR-1进行24h定向RNAi,可获得稳定的大斑块的wasp -1和F-actin。在COR-1的情况下,RNAi的功效反映在皮层的F-actin增加了~40%。gydF4y2BaEgydF4y2Ba-gydF4y2BaHgydF4y2Ba,针对RHO-1, CYK-1, CDC42或CHIN-1的24小时RNAi似乎不影响皮质凝聚物。在针对CDC42和CHIN-1的RNAi情况下,RNAi的功效体现在WSP-1增加了~ 40%和~ 15%。gydF4y2Ba我gydF4y2Ba动态皮质凝析物在NCK-1不活跃的菌株中持续存在。gydF4y2Ba
扩展数据图5中等arx-2 RNAi的体积无关化学计量学演化也设定了内部浓度。gydF4y2Ba
一个gydF4y2Ba,体积vs. f -肌动蛋白体积分数相肖像通过变量的温和变化gydF4y2Baarx-2gydF4y2BaRNAi数据如图所示。gydF4y2Ba3.gydF4y2Ba.橙灰色箭头,如图所示。gydF4y2Ba2摄氏度gydF4y2Ba.黄绿蓝,用经验确定的增长规律计算。颜色表示时间速率变化矢量大小。有效f -肌动蛋白体积分数的时间演化与体积无关(另见补充)。gydF4y2BaBgydF4y2Ba,体积变化率(蓝红热图)作为瞬时体积和有效f -肌动蛋白体积分数的函数。凝析液在f -肌动蛋白有效体积分数为0.5(橙色虚线)时由增长向收缩转变,这对应于转变区域内动力学缓慢的区域(图2)。gydF4y2Ba二维gydF4y2Ba,无花果。gydF4y2Ba4 c, dgydF4y2Ba).gydF4y2BaCgydF4y2Ba,质量通量相像电流大小。等高线(68%,25%)描述了最常用的总强度值。橙色虚线表示转换区域中心对应的有效f -肌动蛋白体积分数(图2)。gydF4y2Ba二维gydF4y2Ba),并与最低电流和最慢动力学相吻合。gydF4y2BaDgydF4y2Ba,浓度磁通相像电流大小。等高线(68%,25%)描述了最常用的浓度值,反映了一对浓度的优先维持。这对浓度位于总密度恒定线(黄色)和主要化学计量线(橙色)的交点上,主要化学计量线对应于(gydF4y2Ba一个gydF4y2Ba-gydF4y2BaCgydF4y2Ba)和图的过渡区域。gydF4y2Ba二维gydF4y2Ba.gydF4y2Ba
图6生长规律建议的粗粒度示意图。gydF4y2Ba
卵母细胞皮层形成示意图,中间阶段有wasp -1、ARP2/3复合物和f -肌动蛋白凝聚物。凝析液动态不稳定的四个过程是:wp -1自我募集、分支依赖的wp -1损失、分支依赖的F-actin增长和F-actin损失(由ARP2/3调节的解聚或切断)。的影响gydF4y2Baarx-2gydF4y2Ba说明了RNAi对f -肌动蛋白损失系数的影响。由于速率系数反映了所有影响组分依赖性凝析液生长的过程的总和效应,分子机制可能涉及更多,但保持所描绘的整体结构。gydF4y2Ba
扩展数据图7过渡到无界增长,和救援事件。gydF4y2Ba
一个gydF4y2Ba,在非rnai对照的卵母细胞和经过18-20hrs处理的卵母细胞中,每个卵母细胞的稳定状态凝聚体数量gydF4y2Baarx-2gydF4y2Ba使用RNAi对RNAi表型严重程度进行分类-轻度(每个卵母细胞有30 ~ 70个皮层凝聚物)和中度(每个卵母细胞有70 ~ 120个皮层凝聚物)gydF4y2Baarx-2gydF4y2BaRNAi。gydF4y2BaBgydF4y2Ba,非rnai对照,轻度和中度gydF4y2Baarx-2gydF4y2BaRNAi条件如中所述gydF4y2Ba一个gydF4y2Ba显示出系统性的增长gydF4y2BakgydF4y2BadgydF4y2Ba随着每个卵母细胞皮层凝聚体数量的减少。在gydF4y2Ba一个gydF4y2Ba,gydF4y2BaBgydF4y2Ba对照,轻度和中度数据集包括gydF4y2BangydF4y2Ba= 9,gydF4y2BangydF4y2Ba= 7和gydF4y2BangydF4y2Ba= 7个卵母细胞,误差条对应平均值的标准误差(gydF4y2Ba一个gydF4y2Ba)和95%置信区间的误差幅度(gydF4y2BaBgydF4y2Ba分别)。严重的gydF4y2Baarx-2gydF4y2BaRNAi导致动态皮质凝析液的损失(每个卵母细胞无凝析液),并出现大面积持续的wp -1和f -肌动蛋白斑块,与无界生长一致(图。gydF4y2Ba3 bgydF4y2Ba,对吧)。因此,我们期望的值gydF4y2BakgydF4y2BadgydF4y2Ba在零时,每个卵母细胞的皮质凝析液与的临界值相吻合gydF4y2BakgydF4y2BadgydF4y2Ba在这个点上凝聚动力学变得无界。的y截距值的外推估计值为线性拟合(虚线)gydF4y2BakgydF4y2BadgydF4y2Ba= 0.49±0.04。注意,这个值类似于的临界值gydF4y2BakgydF4y2BadgydF4y2Ba≈0.47,此时零斜线转换位置(其他三个增长系数由中度确定)gydF4y2Baarx-2gydF4y2BaRNAi),此时A-nullcline高于W-nullcline(见图。gydF4y2Ba3 cgydF4y2Ba,对吧;与左、中相比)。在上图中,y轴上的x表示的值gydF4y2BakgydF4y2BadgydF4y2Ba= 0.51用于计算严重的相像gydF4y2Baarx-2gydF4y2BaRNAi(无花果。gydF4y2Ba3 cgydF4y2Ba(右),这是在无界增长体制。gydF4y2BaCgydF4y2Ba,左为图中代表性图像中的救援事件。gydF4y2Ba1 cgydF4y2Ba.前,快照;底部,记录图沿白线显示救援事件(由绿色方框表示)。右,一个有代表性的皮层凝聚物抢救事件显示了两个生长和收缩周期,被抢救分开。,时间序列;中间,波动曲线记录仪;底层,综合wp -1强度。比例尺,10μm。gydF4y2Ba
扩展数据图8 ARP2/3配合物的可选扰动。gydF4y2Ba
一个gydF4y2Ba,gydF4y2BaBgydF4y2Ba的快照(上)和kymographs(下)gydF4y2Ba秀丽隐杆线虫gydF4y2Ba卵母细胞受(gydF4y2Ba一个gydF4y2Ba) CK666药物治疗及(gydF4y2BaBgydF4y2Ba) 24 h arx-5 RNAi(右)。在这两种情况下,24小时gydF4y2Baarx-2gydF4y2BaRNAi(无花果。gydF4y2Ba3 bgydF4y2Ba右图),可见大面积持续斑块的wasp -1和F-actin。比例尺,10µm。gydF4y2Ba
扩展数据图9与环境无关的局部凝析油生长动态的典型例子。gydF4y2Ba
一位代表gydF4y2Ba秀丽隐杆线虫gydF4y2Ba随时间推移的卵母细胞皮层,放大插图显示三个凝聚体(白色箭头)共享相同的局部环境,但表现出成分不同的瞬时生长。另一个例子如图所示。gydF4y2Ba1 dgydF4y2Ba.比例尺,10µm。gydF4y2Ba
扩展数据图10从图中得到的理论和实验相图gydF4y2Ba2摄氏度gydF4y2Ba分别介绍。gydF4y2Ba
一个gydF4y2Ba,非rnai实验相位图,如图。gydF4y2Ba2摄氏度gydF4y2Ba.gydF4y2BaBgydF4y2Ba,非rnai理论相位图见图。gydF4y2Ba2摄氏度gydF4y2Ba.实线表示wasp -1(绿色)和F-actin(洋红色)为零线,虚线表示wasp -1(绿色)和F-actin(洋红色)轻度gydF4y2Baarx-2gydF4y2BaRNAi空线,虚线表示wasp -1(绿色)和F-actin(洋红色)中度gydF4y2Baarx-2gydF4y2BaRNAi nullclines。gydF4y2Ba
补充信息gydF4y2Ba
补充信息gydF4y2Ba
补充方法,注释1-10和参考文献。gydF4y2Ba
补充表1gydF4y2Ba
本研究中使用的转基因菌株:在列出的菌株中,GFP::Utrophin和PH-domain:: GFP是通过敲入转基因产生的,LifeAct::mKate是通过mos1介导的单拷贝插入(MosSCI)产生的,所有其他蛋白质荧光标记都是通过CRISPR诱变从内源性位点表达的,来自a . C. Reymann的工作和Ou Guangxu实验室的慷慨捐赠。gydF4y2Ba
补充视频1gydF4y2Ba
宫内共聚焦旋转圆盘成像gydF4y2Ba秀丽隐杆线虫gydF4y2Ba卵母细胞向胚胎转变。LifeAct::mKate用洋红色标记F-actin,用绿色标记组蛋白H2B::GFP。比例尺,10µm。时间戳(min:s)。gydF4y2Ba
补充视频2gydF4y2Ba
肌动球蛋白皮质在离体C。gydF4y2Ba线虫gydF4y2Ba卵母细胞。LifeAct::mKate用洋红色标记f -肌动蛋白,绿色标记非肌肉肌球蛋白NMY-2::GFP。比例尺,10µm。时间戳(min:s)。gydF4y2Ba
补充视频3gydF4y2Ba
agydF4y2Ba秀丽隐杆线虫gydF4y2Ba正在形成肌动球蛋白皮质的卵母细胞。LifeAct::mKate用洋红色标记F-actin,用绿色内源性标记wasp -1::GFP。比例尺,10µm。时间戳(min:s)。gydF4y2Ba
补充视频4gydF4y2Ba
agydF4y2Ba秀丽隐杆线虫gydF4y2Ba卵母细胞含有WSP-1和ARX-2。内源性标记的sp -1::GFP为绿色,内源性标记的ARX-2::mCherry为蓝色。比例尺,10µm。时间戳(min:s)。gydF4y2Ba
补充视频5gydF4y2Ba
RNAi喂养24 h后卵母细胞ARX-2明显减少。LifeAct::mKate用洋红色标记F-actin,用绿色标记sp -1::GFP。比例尺,10µm。时间戳(min:s)。gydF4y2Ba
补充视频6gydF4y2Ba
RNAi喂养19 h后卵母细胞ARX-2中度耗尽。LifeAct::mKate用洋红色标记F-actin,用绿色标记内源性wasp -1::GFP。比例尺,10µm。时间戳(min:s)。gydF4y2Ba
补充视频7gydF4y2Ba
的SIM-TIRF电影gydF4y2Ba秀丽隐杆线虫gydF4y2Ba卵母细胞。LifeAct::mKate标记f -肌动蛋白为红色,非肌肉肌球蛋白NMY-2::GFP为绿色。比例尺,10µm。时间戳(min:s)。gydF4y2Ba
权利和权限gydF4y2Ba
开放获取gydF4y2Ba本文遵循知识共享署名4.0国际许可协议(Creative Commons Attribution 4.0 International License),允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可中,除非在材料的信用额度中另有说明。如果内容未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。要查看此许可证的副本,请访问gydF4y2Bahttp://creativecommons.org/licenses/by/4.0/gydF4y2Ba.gydF4y2Ba
关于本文gydF4y2Ba
引用本文gydF4y2Ba
Yan, V.T, Narayanan, A, Wiegand, T。gydF4y2Baet al。gydF4y2Ba凝液动态不稳定性协调肌动球蛋白皮层的激活。gydF4y2Ba自然gydF4y2Ba609gydF4y2Ba, 597-604(2022)。https://doi.org/10.1038/s41586-022-05084-3gydF4y2Ba
收到了gydF4y2Ba:gydF4y2Ba
接受gydF4y2Ba:gydF4y2Ba
发表gydF4y2Ba:gydF4y2Ba
发行日期gydF4y2Ba:gydF4y2Ba
DOIgydF4y2Ba:gydF4y2Bahttps://doi.org/10.1038/s41586-022-05084-3gydF4y2Ba
这篇文章被引用gydF4y2Ba
生物化学计时器相在细胞内凝结进出gydF4y2Ba
自然gydF4y2Ba(2022)gydF4y2Ba
评论gydF4y2Ba
通过提交评论,您同意遵守我们的gydF4y2Ba条款gydF4y2Ba而且gydF4y2Ba社区指导原则gydF4y2Ba.如果您发现一些滥用或不符合我们的条款或指导方针,请标记为不适当。gydF4y2Ba