摘要
脑源性神经营养因子(BDNF)是一种运动诱发的神经营养因子,是记忆巩固和认知功能的重要因素。这项研究评估了血浆BDNF水平与社区老年人虚弱之间的关系。分析了韩国虚弱和衰老队列研究中302名70-84岁人群的血浆BDNF水平。30名(9.9%)受试者有虚弱症状。他们年龄更大,痴呆症和抑郁症的患病率比那些没有虚弱的人更高。在虚弱组和非虚弱组之间,男性的比例没有差异。虚弱的参与者血浆BDNF水平明显低于没有虚弱的参与者。虚弱的存在与血浆BDNF水平(优势比0.508,95%置信区间0.304-0.849)以及年龄、血红蛋白、痴呆症和抑郁症的存在显著相关。在对混杂因素进行校正后,血浆BDNF与虚弱之间仍存在显著相关性(0.495,0.281-0.874)。在排除痴呆、抑郁症、中风、糖尿病和骨质疏松症患者后,这种相关性仍然保持一致。 Plasma BDNF levels were significantly associated with frailty in community-dwelling older adults. Our study may suggest the possible role of BDNF as a novel biomarker of frailty.
介绍
脑源性神经营养因子(BDNF)是大脑中最丰富的神经营养因子,调节神经元的生存、分化和突触可塑性1。血浆BDNF的含量被认为部分反映了其在大脑中的分泌2尽管血小板、血管内皮细胞和平滑肌细胞以及活化的巨噬细胞和淋巴细胞等其他潜在来源也会影响其循环水平3.,4。越来越多的证据表明,血液BDNF水平可以作为阿尔茨海默病诊断、预后和治疗监测的生物标志物5。血液BDNF水平与抑郁症的复发和严重程度有关6。此外,循环中的BDNF水平较低与中风的高风险有关,这一点已得到证实7中风后恢复不佳8。此外,低水平的血液BDNF伴随糖代谢受损9骨密度低10。
众所周知,定期锻炼可以降低患心脏代谢疾病、痴呆症和抑郁症的风险11,12,13。最近的研究表明,BDNF可能是连接运动对血管和代谢的好处与保护神经退行性疾病的关键中介11。事实上,人们对运动引起BDNF循环水平变化的来源和机制知之甚少14。BDNF被确定为骨骼肌中的一种收缩诱导蛋白,因为它已被证明是由骨骼肌在运动时产生的,并通过激活amp活化蛋白激酶(AMPK)来增强骨骼肌中的脂质氧化。15。然而,骨骼肌在运动过程中合成的BDNF以自分泌和旁分泌的方式作用于肌肉15。有趣的是,运动刺激合成纤维连接蛋白III型结构域蛋白5 (FNDC5)及其裂解的循环形式鸢尾素,这可能穿过血脑屏障并诱导BDNF的产生16。在肥胖动物中,BDNF模拟物的管理诱导线粒体生物发生,促进骨骼肌中的脂质氧化,并缓解代谢紊乱17。运动训练后,血清BDNF水平显著升高18。最近的人体研究证实了血液BDNF与骨骼肌功能的相关性。心力衰竭患者血清BDNF与骨骼肌力量呈正相关,而与肌肉质量不相关19。此外,在日本血液透析患者中,BDNF的下降与肌肉力量和身体表现的恶化有关20.。
衰弱,在多个生理系统中储备和抵抗压力源下降的临床综合征,在老年人中很常见21。因此,虚弱与不良结果相关,包括流行的心血管疾病(CVD)和死亡率22,23。Fried等人。21定义了一种虚弱的临床表型,其中存在以下五个标准中的三个或更多:无意的体重减轻,自我报告的疲惫,虚弱,缓慢和低体力活动。因此,老年人肌肉质量和功能的丧失会导致更容易虚弱。尽管血液BDNF可能在肌肉功能中发挥作用,但循环BDNF与虚弱之间的关系尚未完全阐明。对衰弱生物标记物的探索可能有助于早期识别有衰弱的老年人,并在干预期间更容易监测24。因此,我们的目的是调查血浆BDNF水平是否与社区居住的韩国老年人的虚弱相关。我们还进行了敏感性分析,以排除患有bndf相关共病的个体,包括痴呆、抑郁症、中风、糖尿病、心血管疾病和骨质疏松症。
结果
研究对象特征
本研究共纳入302名参与者,中位年龄75岁(IQR 73-79岁)。其中身体虚弱者30人(9.33%)。研究人群的基线特征见表1。体弱组年龄高于非体弱组。男性、当前吸烟者、经常饮酒者和低收入者的比例没有差异;BMI和血压;TC、FPG、HOMA-IR、hs-CRP、血红蛋白、肌酐;在糖尿病、高血压、血脂异常和肥胖的患病率上,介于体弱组和非体弱组之间。然而,与无体弱者相比,体弱者痴呆(40% vs. 14%, P < 0.001)和抑郁症(43.3% vs. 13.6%, P < 0.001)的比例更高。
患者血浆BDNF水平的变化
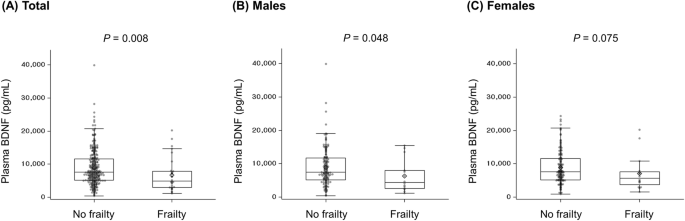
虚弱患者的血浆BDNF水平明显低于无虚弱患者(中位[IQR]: 4.94 [3.02, 7.91] vs. 7.54 [5.19, 11.60] ng/mL, P = 0.008)1,无花果。1).按性别划分时,与对照组相比,体弱受试者血浆BDNF水平较低,但在女性中无统计学意义(图2)。1).
血浆BDNF水平与虚弱之间的关系
接下来,我们进行了单变量和多变量logistic分析,以确定虚弱的存在与血浆BDNF浓度和代谢参数之间的关系2).在单因素分析中,血浆BDNF的增加与虚弱风险降低相关(优势比[OR] 0.508, 95%可信区间[CI] 0.304-0.849,P= 0.01)。另一方面,年龄的增长和痴呆症或抑郁症的存在与虚弱的风险增加有关。在对混杂因素进行调整后,血浆BDNF与虚弱之间的相关性在多因素分析中仍然存在(OR 0.495, 95% CI 0.281-0.874,P= 0.015)。
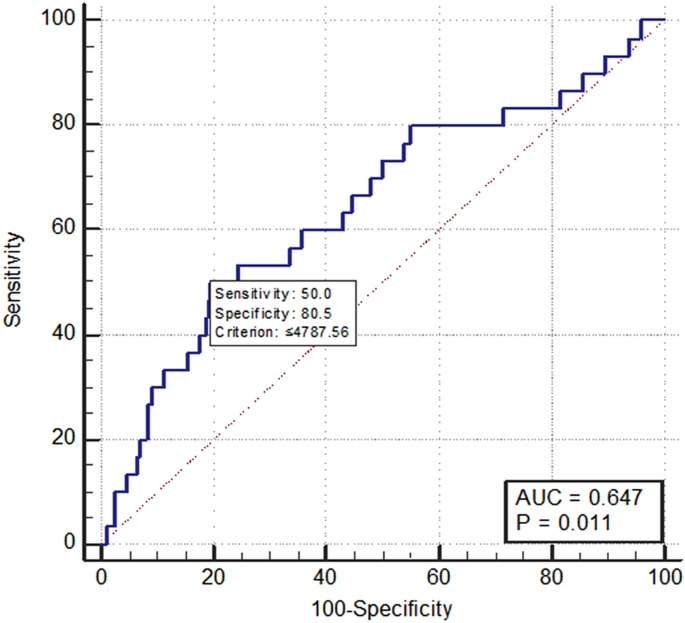
已知循环BDNF水平的改变与代谢和神经精神疾病有关,包括痴呆、抑郁症、中风、糖尿病、心血管疾病和骨质疏松症6,7,8,10,25。因此,通过排除这些共病的参与者进行敏感性分析(补充表)1),结果一致。ROC分析用于评估BDNF预测衰弱的敏感性和特异性(图2)。2).BDNF预测衰弱的最佳临界值≤4.79 ng/ml,敏感性50%,特异性80.5%(曲线下面积0.647,95% CI 0.590 ~ 0.701,P= 0.011)。
讨论
在目前的研究中,在社区居住的老年人中,血浆BDNF水平在患有虚弱的个体中显著低于那些没有虚弱的人。我们还发现,血浆BNDF与虚弱显著相关,无论是否存在痴呆症或抑郁症。有趣的是,血浆BDNF与虚弱之间的联系即使在排除痴呆、抑郁症和代谢障碍(包括中风、糖尿病、心血管疾病和骨质疏松症)的影响后仍然存在。
BDNF在中枢神经系统的发育和功能中起着至关重要的作用。众所周知,BDNF功能障碍参与了多种神经系统疾病和精神疾病的进展,如阿尔茨海默病、中风和抑郁症5,6,7,8。BDNF与受体酪氨酸激酶TrkB相互作用,激活下游细胞内信号通路:主要是磷脂酰肌醇3-激酶(PI3K)/Akt和丝裂原激活蛋白激酶/细胞外信号调节激酶(MAPK/ERK)通路26此外,BDNF是一种重要的炎症调节因子,并通过NF-κ b依赖通路增强大鼠皮质神经元中sestrin2的表达,具有抗氧化作用27。越来越多的证据还表明,氧化应激在神经退行性疾病和精神疾病的病理生理学中导致BDNF功能障碍28。BNDF通过调控某些转录因子的活性,促进神经元的分化、存活和再生。因此,BDNF在阿尔茨海默病、中风和抑郁症中的潜在治疗价值已被广泛研究29。BDNF下调导致阿尔茨海默病中神经毒性淀粉样蛋白β诱导的氧化应激和功能障碍的神经元易感性11。循环BDNF来源于中心源和外围源3.,4,因为BDNF可以双向穿过血脑屏障30.。关于血液BDNF作为痴呆症、抑郁症和中风的生物标志物的价值,已经进行了许多研究5,6,7,8。与以往的研究一致,我们在这项全国性多中心研究中证实血浆BDNF与痴呆症和抑郁症的存在有关。
BDNF和TrkB信号在下丘脑中对摄食行为和能量稳态起作用31,32。BDNF杂合小鼠在成年早期表现出进食行为或运动活动异常,并出现增生和肥胖33。此外,BDNF对糖尿病患者的糖代谢和胰岛素敏感性有良好的影响db / db但BDNF的这些作用并不仅仅依赖于食物摄入量34,35。在人类中,2型糖尿病患者的BDNF循环水平较低,血浆BDNF水平较低与胰岛素抵抗的严重程度相关9。在他们的研究中,在高血糖箝位条件下,脑BDNF输出被取消,导致血浆BDNF水平下降。另一项队列研究也表明,低水平的BDNF是糖尿病和肥胖的独立危险因素25,36。另一方面,年龄大于65岁的糖尿病患者比非糖尿病患者更有可能有更高的衰弱患病率37,38。在本研究中,即使排除了糖尿病患者,BDNF和虚弱之间的联系仍然存在。
此外,BDNF可能是连接运动对血管和代谢的好处与预防神经退行性疾病的关键中介11。运动诱导BDNF循环水平增加的来源和机制尚不清楚14。BDNF是一种收缩诱导的肌细胞来源蛋白,可通过激活AMPK来增加骨骼肌的脂质氧化15。然而,在体育锻炼中,肌肉来源的BDNF以自分泌和旁分泌的方式作用于肌肉,不释放到循环中15。众所周知,血小板通过血液循环从其他来源吸收BDNF,储存它,并在创伤性肌肉损伤等刺激时释放它4。此外,运动能够增加大脑各区域的BDNF,以及循环BDNF水平18,部分是通过诱导FNDC5及其裂解和分泌形式鸢尾素16。因此,有人提出,循环BDNF水平反映了大脑在运动反应中分泌的BDNF39。最近,有报道称,在心力衰竭患者中,较低的血液BDNF水平与骨骼肌力量和身体表现有关,但与肌肉质量无关19还有血液透析患者20.。虽然老年人肌肉质量和功能的丧失可能是虚弱的前兆,但关于血浆BDNF浓度与虚弱之间关系的研究很少。在巴西老年妇女中,血浆BDNF浓度随着Fried weak Phenotype的测定而降低,并且通过锻炼,血浆BDNF水平恢复正常18。此外,血浆BDNF水平与根据日本版CHS标准在日本血液透析患者中定义的虚弱相关20.。然而,这些研究基于少数受试者和特定群体,没有评估心脏代谢变量的影响以及相关慢性疾病的影响,如痴呆、抑郁症、中风、糖尿病、心血管疾病和骨质疏松症。在本研究中,我们观察到血浆BDNF水平在虚弱的参与者中显著降低。此外,即使在广泛调整了包括年龄和神经退行性疾病在内的混杂因素后,虚弱的存在与血浆BDNF水平显著相关。由于在ROC分析中血浆BDNF预测虚弱的敏感性较低,因此有必要将BDNF与其他几个虚弱危险因素一起使用,以提高敏感性和特异性,以提高BDNF作为虚弱筛查试验的有效性。循环BDNF水平已被证明随着年龄的增长而下降24。在排除痴呆、抑郁症和胰岛素抵抗相关代谢疾病(与BDNF密切相关)后的敏感性分析中,保持了相关性。
我们的研究有一些局限性。由于横断面研究设计的内在局限性,我们无法确定血浆BDNF与虚弱之间是否存在因果关系。BDNF水平的下降伴随着肌肉力量和身体机能的丧失,这是由体力活动的减少和衰老引起的,因此,它被认为是导致虚弱的发展的原因。考虑到氧化应激和衰弱之间的联系以及氧化应激在BDNF功能障碍中的重要性28,40, BDNF与氧化应激的相互作用可能有助于衰弱的发病机制。BDNF和TkrB信号通路在衰弱发展中发挥作用的潜在机制有待进一步研究。本研究的另一个局限性是,我们的研究仅限于韩国男性和女性。因此,我们的研究结果很难适用于不同的民族。尽管如此,本研究受益于使用KFACS队列数据库中具有全国代表性的多中心社区老年韩国成年人样本。此外,调整各种混杂因素后的多变量分析和广泛的敏感性分析显示了一致的结果,这可能支持本研究结果的稳健性。
结论
我们在韩国社区老年人中观察到血浆BDNF水平与虚弱之间的关联。虚弱的参与者血浆BDNF水平明显低于没有虚弱的参与者。我们还发现血浆BNDF水平与虚弱之间存在显著相关性,即使在排除患有bdnf相关代谢和神经精神疾病(如痴呆、抑郁症、糖尿病、心血管疾病、中风和骨质疏松症)的参与者后也是如此。因此,我们的研究结果可能提示BDNF作为一种新的虚弱生物标志物的可能作用。
方法
数据来源和研究人群
本研究使用韩国虚弱和老龄化队列研究(KFACS)的数据进行,该研究采用按年龄和性别分层的配额抽样方法,从全国10个不同的医疗中心招募70-84岁的社区居民成年人41。在2017年KFACS招募的1455名参与者中,共有717人根据以下排除标准被纳入:男性每周饮酒> 14杯和> 7每周饮料(n = 463)的女性,慢性肝脏疾病,包括病毒性肝炎和天冬氨酸转氨酶(AST)、丙氨酸转氨酶(ALT)水平大于两倍的正常水平的上限(n = 21),血肌酐水平> 1.5 mg / dL (n = 25),任何炎性疾病与白细胞计数> 10000 /μL (n = 16),任何一种癌症(n = 19),以及使用生物阻抗分析(BIA)而不是双能x射线吸收仪(DXA)测量的身体成分数据(n = 194)。在剩余的717名参与者中,随机选择317人进行血浆BDNF水平分析。最终的分析包括302名参与者,其中15名参与者在现场采访中缺少关于病史和生活方式因素和实验室测量的数据。
脆弱评估
脆弱是使用油炸脆弱表型定义的,也称为心血管健康研究(CHS)脆弱表型21有修改过的截断41,包括五个虚弱的组成部分:无意识的体重减轻(过去一年4.5公斤),自我报告的疲惫,虚弱(握力),缓慢的步行速度和低体力活动。上述五个组成部分的详细信息已在前面介绍过41。用数字手握力测定仪(Takei TKK 5401;Takei Scientific Instruments Co., Tokyo, Japan),并使用最高值进行分析。步速是使用自动计时器(Gaitspeedometer;动态生理学,大田,韩国),加速和减速阶段为1.5米。使用国际体育活动问卷(IPAQ)确定体育活动水平(千卡/周),并根据问卷中的剧烈、中度和轻度活动得出代谢当量分数。通过将上述五个组成部分的积极反应赋值为1来计算CHS脆弱总分(范围:0-5)。总分为3-5分的参与者被认为是虚弱的,总分为0-2分的参与者被认为是非虚弱的。
实验室测量
在每个中心禁食8小时后,大约上午8点采集血液样本,并运送到核心实验室(Seegene Inc.,首尔,韩国)。离心后,血浆样本储存在深冷冻室中,直到分析。血液化学测试包括空腹血糖(FPG)、总胆固醇(TC)、肌酐、血红蛋白和高敏c反应蛋白(hs-CRP),除血浆胰岛素外,使用Cobas 8000 C702分析仪(Roche Diagnostics, Mannheim, Germany)进行。使用Cobas 8000 e602分析仪(Roche Diagnostics)分析血浆胰岛素,使用Tosoh HLC-723 G8分析仪(Tosoh Corporation, Tokyo, Japan)测量糖化血红蛋白水平。采用以下公式计算稳态模型评估-胰岛素抵抗(HOMA-IR):空腹血糖(mmol/L)乘以空腹血清胰岛素(mU/L)除以40542。血浆BDNF水平使用定量夹心酶联免疫吸附测定试剂盒(目录编号:;bek - 2211;Biosensis, Thebarton,澳大利亚)。
其他变量和定义
在访问期间,测量了参与者的体重、身高以及收缩压和舒张压(分别为SBP和DBP)。体重指数(BMI)的计算方法为体重(kg)除以身高(米)的平方(m)2).通过现场访谈评估参与者的年龄、性别、吸烟状况、饮酒、体育活动、收入和病史(包括既往诊断为糖尿病、高血压、血脂异常、中风、心绞痛、心肌梗死和骨质疏松症)。经常饮酒定义为每周饮酒≥2次。收入水平在较低的20%水平上被一分为二。肥胖定义为BMI≥25 kg/m2。慢性肾病定义为肾小球滤过率< 60 mL/min/1.73 m2由慢性肾脏疾病流行病学协进会Eq。43。糖尿病定义为FPG≥126 mg/dL, HbA1c≥6.5%,或既往诊断为糖尿病。CVD的定义是既往诊断为心绞痛和心肌梗死。认知功能评估采用简易精神状态检查(MMSE),痴呆症定义为MMSE评分< 2444。抑郁症是用韩国版的老年抑郁量表(Short Form Geriatric Depression Scale)确定的,评分≥6分45。
统计分析
对于连续变量,数据以均值±标准差或中位数(四分位范围)表示,对于分类变量,数据以计数和百分比(%)表示。使用独立双样本t检验或连续变量的Mann-Whiney u检验和χ比较有和无身体虚弱的参与者的基线特征2测试分类变量。由于血浆BDNF水平呈高度偏态分布,故采用数据的自然对数变换进行统计分析。以体质虚弱为因变量,血浆BNDF值、年龄、性别、BMI、SBP、吸烟、经常饮酒、低收入,以及TC、FPG、HOMA-IR、hs-CRP、血红蛋白、肌酐、痴呆和抑郁症等实验室数据为自变量,进行单因素和多因素logistic回归分析。在多变量逻辑回归模型中,所有在单变量分析中被发现显著的因素都被使用。我们还进行了敏感性分析,以排除bdnf相关共病的影响,如痴呆、抑郁症、中风、糖尿病、心血管疾病和骨质疏松症。受试者工作特征(ROC)分析用于验证血浆BDNF对评估虚弱的预测有效性。p值< 0.05在整个分析过程中被认为具有统计学意义。所有统计分析均由经验丰富的专业统计学家使用SAS 9.4版本(SAS Institute Inc., Cary, NC, USA)进行。
道德
这项研究是根据1964年的赫尔辛基宣言进行的。KFACS的研究方案得到了高丽大学九老医院机构审查委员会(批准号)的批准。2020 gr0139)。所有参与者均获得书面知情同意。
数据可用性
用于支持本研究结果的数据可根据合理要求从通讯作者处获得。
缩写
- 体重指数:
-
身体质量指数
- 脑源性神经营养因子:
-
脑源性神经营养因子
- CHS:
-
心血管健康研究
- 置信区间:
-
置信区间[CI]
- 心血管疾病:
-
心血管病
- HOMA-IR:
-
稳态模型评估-胰岛素抵抗
- hs-CRP:
-
高敏c反应蛋白
- KFACS:
-
韩国人虚弱与衰老队列研究
- 或者:
-
优势比
参考文献
黄,E. J. & Reichardt, L. F.神经营养因子:在神经元发育和功能中的作用。为基础。启>。24, 677-736(2001)。
Lommatzsch, M。et al。年龄、体重和性别对人类血小板和血浆中BDNF水平的影响。一般人。老化26, 115-123(2005)。
Nakahashi, T。et al。血管内皮细胞合成和分泌脑源性神经营养因子。2月。470, 113-117(2000)。
》,H。et al。脑源性神经营养因子储存在人的血小板中,经激动剂刺激释放。Thromb。Haemost。87, 728-734(2002)。
宋俊华,于俊涛,谭丽娟。脑源性神经营养因子在阿尔茨海默病中的作用:风险、机制与治疗。摩尔。一般人。52, 1477-1493(2015)。
戴尔'Osso, L。et al。脑源性神经营养因子血浆水平与抑郁症患者疾病严重程度、复发和症状之间的关系Neuropsychobiology62, 207-212(2010)。
Pikula,。et al。血清脑源性神经营养因子和血管内皮生长因子水平与卒中和血管性脑损伤风险相关:弗雷明汉研究中风44, 2768-2775(2013)。
斯坦恩t.m.et al。低循环急性脑源性神经营养因子水平与缺血性卒中后不良的长期功能预后相关。中风47, 1943-1945(2016)。
Krabbe, k.s.。et al。脑源性神经营养因子(BDNF)和2型糖尿病。Diabetologia50, 431-438(2007)。
鼻子,S。et al。闭经和经期运动员血清脑源性神经营养因子水平反映骨密度。Int。J.运动医学40, 276-282(2019)。
王,R. & Holsinger, R. M. D.运动诱导的脑源性神经营养因子表达:阿尔茨海默氏症的治疗意义。老化决议案48, 109-121(2018)。
Demurtas, J。et al。轻度认知障碍和痴呆患者的身体活动和锻炼:干预和观察性研究的综合综述。j。地中海,Dir。Assoc。21, 1415 - 1422。e1416(2020)。
荣格,我。et al。新诊断糖尿病患者体力活动模式的改变与心力衰竭风险糖尿病金属底座。J。46, 327-336(2022)。
沃尔什,J. J. & Tschakovsky, m.e.运动和循环BDNF:释放机制和运动干预设计的意义。达成。杂志。减轻。金属底座。43, 1095-1104(2018)。
马修斯,V. B.;et al。脑源性神经营养因子是由骨骼肌细胞在收缩时产生的,通过激活amp活化蛋白激酶促进脂肪氧化。Diabetologia52, 1409-1418(2009)。
弗兰,c.d.。et al。运动通过PGC-1alpha/FNDC5途径诱导海马BDNF。细胞金属底座。18, 649-659(2013)。
木头,J。et al。BDNF模拟物通过增强骨骼肌线粒体生物发生来缓解肥胖小鼠的体重增加。新陈代谢87, 113-122(2018)。
科埃略,f.m.et al。物理治疗干预(PTI)增加血浆脑源性神经营养因子(BDNF)水平在非虚弱和前期虚弱的老年妇女。拱门。Gerontol。Geriatr。54, 415-420(2012)。
Nakano,我。et al。心衰患者血清脑源性神经营养因子水平与骨骼肌功能相关,但与肌肉质量无关。Int。心J。61, 96-102(2020)。
Miyazaki, S., Iino, N., Koda, R., Narita, I. & Kaneko, Y.脑源性神经营养因子与日本血液透析患者的肌肉减少症和虚弱有关。Geriatr。Gerontol。Int。21, 27-33(2021)。
弗里德,l.p.。et al。老年人的虚弱:表型的证据。j . Gerontol。一个杂志。科学。医学科学。56, m146-156(2001)。
考森,p。et al。老年男性虚弱:患病率、进展及与死亡率的关系。j。Geriatr。Soc。55, 1216-1223(2007)。
新近,J。et al。老年人心血管护理中的虚弱评估。j。科尔。心功能杂志。63, 747-762(2014)。
凯恩,A. E. &辛克莱,D. A.人类和啮齿动物的脆弱生物标志物:目前的方法和未来的进展。动力机械。老化的开发。180, 117-128(2019)。
李,B.,郎,N.,程志峰。血清脑源性神经营养因子水平与糖尿病风险、并发症和肥胖相关:一项来自中国2型糖尿病患者的队列研究。摩尔。一般人。53, 5492-5499(2016)。
赵,H。et al。脑源性神经营养因子在神经保护中的分子机制研究进展。大脑Res。1665, 1-21(2017)。
吴春林,陈世东,尹俊华,黄春生,杨德立。核因子kappab诱导的Sestrin2介导BDNF对大鼠皮质神经元线粒体抑制的抗氧化作用。摩尔。一般人。53, 4126-4142(2016)。
张晓勇。et al。慢性精神分裂症中BDNF与氧化应激的相互作用。心理神经内分泌学51, 201-208(2015)。
长原,A. H. & Tuszynski, M. H. BDNF在神经和精神疾病中的潜在治疗用途。Nat. Rev.药物发现10, 209-219(2011)。
潘伟,班克斯,W. A.,法索德,M. B.,布鲁斯,J. &卡斯汀,A.。脑源性神经营养因子通过血脑屏障的运输。神经药理学37, 1553-1561(1998)。
BDNF和喂养的中央控制:偶然的旁观者还是重要的参与者?趋势>。36, 83-90(2013)。
于俊华,金明生。食欲调节的分子机制。糖尿病金属底座。J。36, 391-398(2012)。
Kernie, s.g., Liebl, d.j.和Parada, l.f. BDNF调节小鼠的进食行为和运动活动。EMBO J。19, 1290-1300(2000)。
唐娜,j.r.。et al。脑源性神经营养因子改善C57BLKS-Lepr(db)/lepr(db)小鼠血糖控制,缓解空腹高血糖糖尿病48, 588-594(1999)。
中川,T。et al。脑源性神经营养因子通过调节糖尿病小鼠能量平衡调节糖代谢。糖尿病49, 436-444(2000)。
El-Gharbawy, a。et al。瘦和超重儿童和青少年血清脑源性神经营养因子浓度。j .中国。性。金属底座。91, 3548-3552(2006)。
尹俊伟。et al。高血糖与老年糖尿病男性肌肉质量受损有关:韩国健康与衰老纵向研究糖尿病金属底座。J。40, 140-146(2016)。
彭,P。et al。HOMA-IR与美国中老年人体质衰弱之间的关系。科学。代表。9, 4238(2019)。
拉斯穆森,P。et al。运动时大脑释放脑源性神经营养因子的证据。Exp。杂志。94, 1062-1069(2009)。
单身,M。et al。在老年人群中,氧化应激与虚弱有关,而与年龄或性别无关:脂质和蛋白质氧化作为虚弱的生物标志物。j。Geriatr。Soc。62, 1324-1328(2014)。
温,c.w.et al。韩国虚弱和衰老队列研究(KFACS):队列概况。BMJ开放10, e035573(2020)。
马修斯,博士。et al。稳态模型评估:人空腹血糖和胰岛素浓度的胰岛素抵抗和β细胞功能。Diabetologia28, 412-419(1985)。
慢性肾脏疾病。年报实习生。地中海。162, 1-16(2015)。
O ' donnell M。et al。认知障碍、心血管事件和死亡风险。欧元。心J。33, 1777-1786(2012)。
Bae, J. N.和Cho, M. J.发展的韩国版本的老年抑郁症量表和它的简短形式在老年精神病患者。j . Psychosom。Res。57, 297-305(2004)。
确认
我们非常感谢研究参与者和韩国虚弱和老龄化队列研究的工作人员在这项研究中的合作。
资金
这项研究得到了韩国卫生技术研发项目通过韩国卫生产业发展研究所(KHIDI)的资助,该研究所由卫生部和卫生部资助。福利,大韩民国(资助号:HI15C3153),以及由韩国疾病控制和预防机构国立卫生研究所资助的研究项目(2021-ER0605-00)。这项工作也得到了高丽大学九老医院(韩国研究驱动医院)的支持,高丽大学医学院(K2210431)和韩国教育部资助的韩国国家研究基金会(NRF)的资助(资助号:2020R1I1A1A01070499)。资助者在研究的设计、收集、分析或数据解释或手稿的准备、审查或批准中没有任何作用。
作者信息
作者及隶属关系
贡献
e.r.、m.k.、c.w.w.和K.M.C.构思并设计了这项研究。e.r.、e.s.、m.j.p.、m.k.、c.w.w.和K.M.C.对数据采集有贡献。e.r., s.y.h.和K.M.C.对统计分析有贡献。E.R, H.J.Y, S.H.B, C.W.W.和K.M.C.对数据解释有贡献。E.R, C.W.W和K.M.C.写的手稿。所有作者均已批准提交的稿件。
相应的作者
道德声明
相互竞争的利益
作者声明没有利益竞争。
额外的信息
出版商的注意
施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
补充信息
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/。
关于本文
引用本文
卢娥,黄世英,宋娥。et al。血浆脑源性神经营养因子水平与社区老年人虚弱的关系。Sci代表12, 18605(2022)。https://doi.org/10.1038/s41598-022-19706-3
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s41598-022-19706-3