摘要
急性胰腺炎(AP)患者可能有心血管疾病(CVD)的风险增加。很少有研究涉及糖尿病患者AP与CVD风险之间的关系。本研究旨在通过分析韩国大规模的国家索赔数据库,调查糖尿病和AP病史患者的心血管疾病风险和死亡率。分析了来自韩国国民健康保险服务数据库的数据。在2009年至2012年期间,共有2,746,988名2型糖尿病患者接受了全面健康检查。根据检查前的AP病史(是或否)将参与者分为两组,并分析直到2018年的随访数据。主要终点为卒中、心肌梗死(MI)或死亡的发生。Cox比例危险回归分析用于评估AP病史与卒中、心肌梗死和死亡率之间的关系。排除后,有AP史和无AP史的参与者人数分别为3810人和2258,910人。有AP史的患者中风、心肌梗死和死亡率明显较高。 The adjusted hazard ratios (95% confidence interval) for the risk of stroke, MI, and mortality were 1.534 (1.342–1.753), 1.998 (1.733–2.303), and 2.353 (2.200–2.515), respectively. Age < 65, male sex, current smoking, and drinking significantly increased the risk of death in the subgroup analyses. The risk of stroke, MI, and mortality was significantly higher in diabetic participants with AP history than those without AP history at 9-year follow-up. This suggests that active management of cardiovascular risk factors is necessary in diabetic patients with AP history.
简介
急性胰腺炎(AP)是美国胃肠道疾病中住院治疗的主要原因,造成巨大的经济负担(每年26亿美元)。1.AP的发病率为每10万5 ~ 30例,近年来呈上升趋势2,3..尽管重症急性胰腺炎本身的死亡率很高4最近的研究表明,与对照组相比,AP患者也有更高的心血管疾病(CVD)风险(调整后的危险比[HR], 1.24-1.76)5,6.与AP相关的炎症细胞因子、血流动力学障碍和代谢障碍可能在增加CVD风险中发挥重要作用5.相反,也有报道称CVD可能增加AP的风险7提示在短期和长期内,心血管疾病与AP密切相关。然而,还需要进一步的研究来提出确切的机制。
心血管疾病是世界上公认的主要死亡原因,占死亡人数的32%8.大多数心血管疾病相关的死亡可归因于冠心病或脑血管疾病。AP被认为会通过增加CVD的风险而影响长期发病率和死亡率,也会由于胰腺炎本身的问题而影响短期死亡率。在估计心血管疾病风险的过程中,考虑众所周知的危险因素是至关重要的。特别是,糖尿病是心血管疾病发生的最重要的独立危险因素9.美国糖尿病协会建议对所有糖尿病患者进行系统的、年度的心血管疾病危险因素评估。这些危险因素包括肥胖、高血压、血脂异常、吸烟、早发冠心病史和蛋白尿9.事实上,改变这些危险因素的努力可以显著降低糖尿病患者的长期死亡率和发病率10.
如上所述,虽然AP被认为会增加CVD的风险,但之前的研究并没有考虑吸烟等重要因素5,6.此外,很少有研究涉及糖尿病患者AP与CVD风险之间的关系。在这项研究中,我们旨在通过分析韩国大规模的具有全国代表性的索赔数据库,调查糖尿病和AP病史患者的CVD风险和死亡率。
方法
数据集
分析了来自韩国国民健康保险服务(NHIS)数据库的数据。国民健康保险是一家保险公司,覆盖97%的国民,其数据库包括人口统计信息、医疗索赔、一般健康检查结果、死亡信息等。基于索赔的数据库包括诊断、处方、住院和机构级别的记录,所有这些都是在去身份识别后提供的。一般健康检查包括健康史问卷、测量人体测量指数和血压、禁食一晚后采血、尿检和胸部x光检查。诊断使用了《国际疾病和相关健康问题统计分类第十版》(ICD-10)代码。该研究方案得到了崇实大学制度审查委员会(No。四- 202003 -人力资源- 201 - 01)。崇实大学制度审查委员会的决定免除了书面知情同意的要求。所有的方法都按照相关的指导方针和规定进行。
研究人群
在2009年至2012年期间,共有2,746,988名2型糖尿病(T2DM)患者接受了常规健康检查。年龄在20岁以下的参与者,那些在检查日期(滞后期)之前和之后一年内被诊断为中风或心肌梗死(MI)的参与者,以及那些数据缺失的参与者被排除在研究之外。其余2,264,074名参与者根据考试前三年内的AP病史(是或否)分为两组。收集并分析了这些参与者到2018年的随访记录。在检查日期后没有AP病史的参与者中,新的AP病例被排除在分析之外。参加国家健康检查的人对使用其数据进行研究提供了书面知情同意。仅使用未识别的数据进行分析。
定义
所有诊断均结合ICD-10代码和操作定义进行。T2DM诊断定义如下:(1)存在ICD-10编码E11-E14,并声称基线时至少口服过一种抗糖尿病药物或胰岛素,或(2)一般健康检查结果空腹血糖水平≥126 mg/dL。AP被定义为在同一期间出现代码K85和住院。
这项研究的主要终点是中风、心肌梗死或死亡的发生。由于如果发生卒中、心肌梗死或死亡,则认为终点已达到,因此卒中或心肌梗死死亡不包括在终点内。卒中定义为I63或I64编码,有住院史,并要求进行脑成像(磁共振成像或计算机断层扫描)。MI定义为I21或I22代码的住院。高血压由I10-I13和I15代码定义或收缩压/舒张压≥140/90 mmHg,至少有一种降压药处方要求。血脂异常被定义为每年至少有一起编码为E78或总胆固醇≥240mg /dL的抗高脂血症药物的索赔。定期运动定义为>每周至少5次30分钟的中等强度体育活动或>每周至少3次20分钟的剧烈体育活动。
统计分析
基线特征以数字(%)、平均值±标准差或几何均值(95%置信区间[CI])表示。连续变量采用Student 's t检验,分类变量采用Pearson 's卡方检验。Cox比例危险回归分析用于评估AP病史与中风、心肌梗死和死亡风险之间的关系。在分析过程中,拟合了五个模型以逐渐减少混杂关联。模型1为未调整模型。模型2根据年龄和性别进行了调整。在模型3中,吸烟、饮酒、定期锻炼和收入水平在年龄和性别之后依次添加。共病(高血压和血脂异常)和体重指数(BMI)被添加到模型4中,糖尿病相关变量(糖尿病病程、胰岛素的使用和两种或两种以上口服糖尿病药物的处方)被进一步添加到模型5中。采用7个二元变量(年龄65岁、性别、当前吸烟、饮酒、高血压、血脂异常和BMI 25 kg/m)的模型5进行亚组分析2).这些结果以95% CI的HRs表示。卒中、心肌梗死和死亡率的累积发生率用Kaplan-Meier曲线绘制。统计学意义定义为双侧p值< 0.05。所有统计分析均使用SAS版本9.3 (SAS研究所公司,Cary, NC,美国)和R版本3.2.3 (R统计计算基金会,维也纳,奥地利;http://www.Rproject.org).
伦理批准并同意参与
该研究方案得到了崇实大学制度审查委员会的批准。无需书面知情同意。
结果
基线特征
有和没有AP病史的参与者人数分别为3810人和2258,910人。如表所示1有AP史组年龄、体重指数、腰围、肾功能、血压、胆固醇水平均明显低于无AP史组(对照组)。相反,在有AP史的组中,男性比例、胰岛素的使用、两种或两种以上抗糖尿病药物的摄入量、当前吸烟者、重度饮酒者、低收入参与者以及肝脏相关酶水平显著较高。然而,高血压、血脂异常、长期糖尿病和定期锻炼的参与者在两组之间的比例没有显著差异。
心血管事件的风险和死亡率根据急性胰腺炎的历史
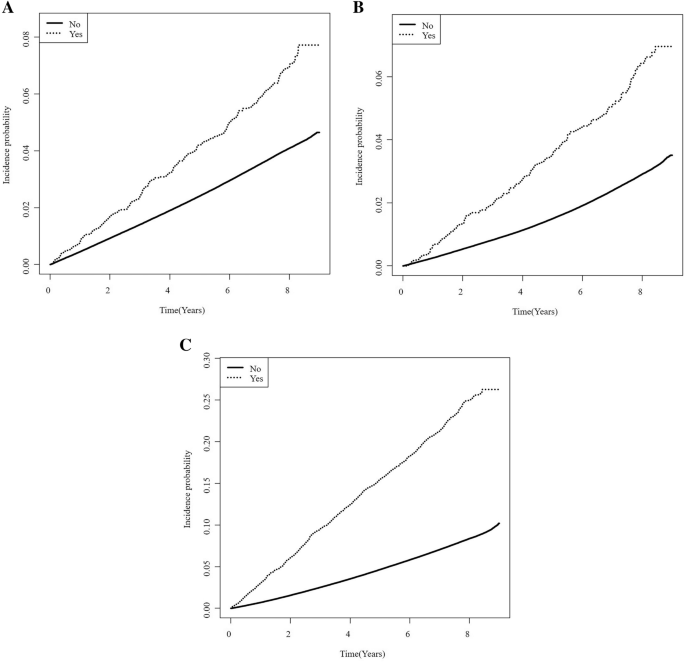
表格2显示Cox比例风险回归分析结果,根据AP病史评估卒中、心肌梗死和死亡率的独立风险。有AP病史的患者中风、心肌梗死和死亡率明显较高。各事件在随访期间发生概率的Kaplan-Meier曲线如图所示。1.所有log-rankp值< 0.0001。卒中、心肌梗死和死亡率的粗hr (95% CI)分别为1.858(1.626-2.123)、2.549(2.212-2.937)和3.500(3.274-3.741)。在调整年龄和性别后(模型2),除中风外,HRs略有下降。经社会因素(模型3)和共病因素(模型4)调整后,各事件的危险度进一步降低,其中死亡率危险度降低最多。在最终模型中调整糖尿病相关变量后,注意到所有事件的hr总体上降低最多。在最后的模型(模型5)中,与对照组相比,AP病史仍然会使中风、心肌梗死和死亡率分别增加1.5倍、2.0倍和2.4倍。
亚组心血管事件和死亡率的风险
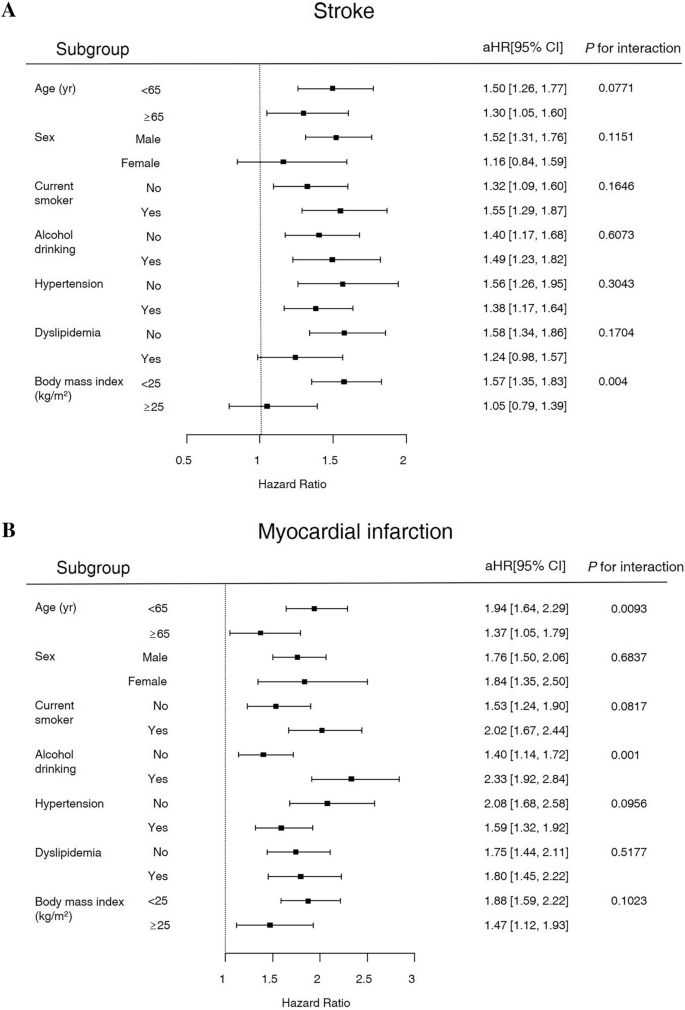
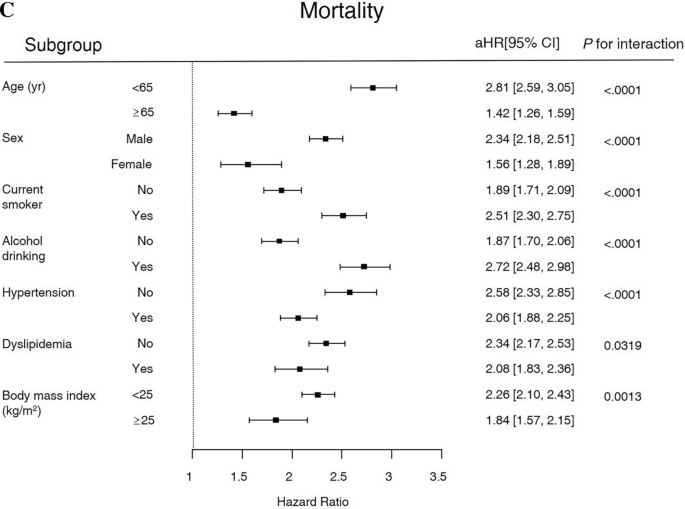
中风、心肌梗死风险和死亡率按年龄、性别、吸烟、饮酒、高血压、血脂异常和BMI进行亚组分析的结果见图。2.在有AP病史的受试者中,BMI < 25 kg/m的受试者中风风险显著较高2.心肌梗死的风险在年龄< 65岁且饮酒的人群中显著增高。在死亡率方面,年龄< 65岁、男性、目前吸烟和饮酒显著增加死亡风险。此外,低BMI、无高血压或血脂异常会增加有AP病史的糖尿病患者的死亡率。
讨论
在这项大规模的全国性队列研究中,在10年随访中,有AP史的糖尿病患者中风、心肌梗死和死亡率的独立风险显著高于无AP史的糖尿病患者。在考虑重要混杂变量后,调整后的HRs为1.5 ~ 2.4。本研究结果提示,对于有AP病史的糖尿病患者,积极管理心血管危险因素是必要的。
最近一项类似的大规模队列研究报道,AP患者的急性CVD调整后HR为1.76 (95% CI, 1.47-2.12),这与我们的结果相当5.然而,与我们的研究不同,该报告没有调整吸烟和酒精等重要的混杂因素。此外,该报告没有考虑研究期间AP发生和CVD的时间顺序,难以评估因果关系。相比之下,我们的研究显示了一种可能的因果关系,因为我们构建了一个单独的有AP病史但没有CVD的糖尿病患者队列,并进行了长期随访,以评估CVD发病率或死亡率。另一项类似的队列研究表明,首次AP患者发生急性冠状动脉综合征的风险高于无AP患者(糖尿病患者调整后的HR为2.46)。6.该研究还表明,大约三分之一的急性冠状动脉综合征是在AP发生的一个月内发生的。然而,该研究没有包括滞后期,这意味着在AP前纳入许多CVD患者的可能性。此外,该研究也没有调整吸烟或BMI等重要因素。
AP是一种急性全身性炎症过程,在不同程度上涉及一个或多个器官系统11.特别是心血管系统在AP的所有阶段都可能受到影响,包括血流动力学、心律和心包变化。因此,在AP早期,液体复苏非常重要12,13,14.AP也被认为与微循环障碍有关15.我们认为,这些变化在短期内对心血管结局起着重要作用,并可能在长期内通过动脉粥样硬化影响CVD的发生5.AP过程中几种炎性细胞因子如肿瘤坏死因子α、白介素-6、IL-10和趋化因子单核细胞趋化蛋白-1的释放16可能与动脉粥样硬化的发病机制有关17,18.然而,需要更多的研究来阐明确切的机制。
如表所示1有AP病史的糖尿病患者通常需要胰岛素或其他抗糖尿病药物。这表明AP可能与内分泌功能障碍的水平有关,内分泌功能障碍似乎影响糖尿病的严重程度,而糖尿病的严重程度又可能增加心血管疾病的风险。先前的一项荟萃分析显示,AP后37%的个体观察到前驱糖尿病和/或DM,诊断后5年的相对风险为2.719.因此,有AP病史的糖尿病患者中,很大一部分可能属于胰源性或3c型糖尿病20..然而,在我们的研究中很难确认AP和糖尿病之间的因果关系,因为我们确定了在基线时有AP病史的糖尿病患者。
Cox比例风险回归分析显示,HR最高的是全因死亡率(2.353),其次是心肌梗死(1.998)和中风(1.534)(表5)2).在有AP病史的参与者中,CVD每1000人年的简单发生率为16.76,全因死亡率为34.88。因此,预计除了心血管疾病之外,还存在其他导致死亡率的因素。虽然我们还不能调查每个患者的死亡原因,但可能有患者死于各种恶性肿瘤,这些肿瘤已知会随着糖尿病而增加,特别是在诊断为AP后胰腺癌的风险增加21.此外,也可能有患者死于其他致命的糖尿病并发症,如感染或终末期肾病22.有趣的是,亚组分析显示,没有高血压或血脂异常的年轻参与者(< 65岁)的死亡率更高(图2)。2).结合这些结果,我们注意到AP发生在较年轻的年龄时,长期预后较差。在这种情况下,心血管疾病以外的疾病可能对死亡率有显著影响。早期经历AP事件的饮酒者更有可能从AP发展为慢性胰腺炎(CP)23.已知AP进展为CP时死亡率较高24因此,与AP-CP序列相关的几个因素可能在我们的研究中极大地促进了年轻参与者死亡率的增加。然而,由于在我们的研究中没有将CP的发生作为结果进行评估,因此很难确定CP的实质性影响。
事实上,在上述研究中,CP患者发生CVD的风险(调整后HR为3.42)高于AP患者(调整后HR为1.76)5.在其他研究中也报道了CP患者CVD风险增加,范围为1.27-1.45325,26,27.然而,由于CP患者的异质性,在解释结果时需要谨慎。关于基于索赔数据的研究,如我们的研究,仅使用诊断代码很可能无法正确识别真正的CP患者。我们认为,要对CP进行所谓的大数据研究,需要更细致的操作性定义。因此,我们认识到CP很难作为研究结果。
我们的研究有几个局限性。首先,结果可能取决于AP的病因和严重程度,这在我们的研究中没有考虑到。这是NHIS数据库的一个内在限制。第二,如上所述,AP后发生糖尿病的参与者很可能被诊断为3c型糖尿病而不是T2DM。然而,很难确定本研究中包括的这类参与者的数量。第三,我们没有考虑给参与者使用的药物。在糖尿病患者中,抗血栓药物等药物28,29或二甲双胍5,30.可能影响心血管结局和死亡率。第四,我们没有评估其他属于心血管疾病范畴的疾病,如心绞痛、心力衰竭或外周动脉疾病31.最后,两组的一些特征如基线特征(包括年龄、BMI、饮酒和吸烟史)有统计学上的显著差异,这些特征直接影响CVD。此外,从调查中获得的有关吸烟和饮酒的信息可能被低估了。这些因素很难通过匹配来控制,因为AP和CVD有许多共同的危险因素。AP似乎发挥了一定的作用,因为即使我们用Cox比例风险比法调整了混杂因素,我们也能获得显著的结果。尽管如此,我们的研究的优势在于,我们提出了心血管疾病的风险和死亡率,通过长期随访调整重要的混杂变量,根据相对统一和大量的糖尿病参与者的AP病史,他们进行了健康检查。
结论
这项大规模的全国性队列研究表明,有AP史的糖尿病患者CVD风险和死亡率显著增加。对于糖尿病患者的风险管理,检查AP病史和主要心血管危险因素是至关重要的。为了充分解释这种增加的风险,未来需要对胰源性糖尿病患者进行准确的考虑,并对AP对心血管系统和代谢成分的长期影响进行详细的研究。
数据可用性
根据合理要求,本研究中产生的衍生数据可从相应作者处获得。
缩写
- 记者:
-
急性胰腺炎
- 体重指数:
-
身体质量指数
- 置信区间:
-
置信区间
- CP:
-
慢性胰腺炎
- 心血管疾病:
-
心血管病
- 人力资源:
-
风险比
- 诊断结果:
-
《疾病及相关健康问题国际统计分类》第十版
- IL:
-
白介素
- 小姐:
-
心肌梗死
- 简介:
-
国民健康保险制度
- 2型糖尿病:
-
2型糖尿病
参考文献
Peery, A. F。et al。美国胃肠道、肝脏和胰腺疾病的负担。胃肠病学149(7), 1731-1741(2015)。
Fagenholz, P. J., Castillo, C. F., Harris, N. S., Pelletier, A. J. & Camargo, C. A. Jr.增加美国急性胰腺炎住院率,1988-2003。安。论文。17(7), 491-497(2007)。
Krishna, s.g., Kamboj, a.k., Hart, p.a., Hinton, A. & Conwell, d.l.急性胰腺炎住院流行病学的变化:十年趋势和慢性胰腺炎的影响。胰腺46(4), 482-488(2017)。
Johnson, C. D. & Abu-Hilal, M.第一周内持续器官衰竭是急性胰腺炎致命结局的标志。肠道53(9), 1340-1344(2004)。
宋,l.c.。et al。急性和慢性胰腺炎患者发生急性动脉粥样硬化性心血管疾病的风险科学。代表。11(1), 20907(2021)。
Chung, W. S. & Lin, C. L.急性胰腺炎患者急性冠状动脉综合征的发生率和风险:一项全国性队列研究。Pancreatology17(5), 675-680(2017)。
Bexelius, T. S., Ljung, R., Mattsson, F. & Lagergren, J.心血管疾病与急性胰腺炎风险在一项基于人群的研究中。胰腺42(6), 1011-1015(2013)。
死亡原因C: 1990-2013年全球、区域和国家240种死亡原因的按年龄性别划分的全因和按原因划分的死亡率:2013年全球疾病负担研究的系统分析。《柳叶刀》385(9963), 117-171(2015)。
A.美国糖尿病心血管疾病和风险管理:糖尿病医疗保健标准-2021。糖尿病护理44(1), s125-s150(2021)。
Gaede, P., Lund-Andersen, H., Parving, H. H. & Pedersen, O.多因素干预对2型糖尿病死亡率的影响。心血管病。j .地中海。358(6), 580-591(2008)。
Yegneswaran, B, Kostis, J. B. & Pitchumoni, C. S.急性胰腺炎的心血管表现。j .暴击。护理26(2)、225. e211 - 225。e228(2011)。
巴克斯鲍姆,j.l.。et al。早期侵袭性水合加速轻度急性胰腺炎的临床改善。点。j .杂志。112(5), 797-803(2017)。
沃恩多夫,m.g.。et al。早期液体复苏可降低急性胰腺炎患者的发病率。中国。杂志。乙醇。掉了。中国。Pract。j。杂志。Assoc。9(8), 705-709(2011)。
加德纳,t.b.。et al。急性重症胰腺炎早期快速液体复苏可降低住院死亡率。Pancreatology9(6), 770-776(2009)。
Cuthbertson, C. M. & Christophi .急性胰腺炎微循环障碍。Br。j .杂志。93(5), 518-530(2006)。
急性和慢性胰腺炎的炎症。咕咕叫。当今。杂志。31(5), 395-399(2015)。
Ramji, D. P. & Davies, T. S.动脉粥样硬化中的细胞因子:疾病所有阶段的关键参与者和有希望的治疗靶点。细胞因子生长因子Rev。26(6), 673-685(2015)。
Tousoulis, D., Oikonomou, E., Economou, E. K. Crea, F. & Kaski, J. C.动脉粥样硬化中的炎症细胞因子:当前的治疗方法。欧元。心J。37(22), 1723-1732(2016)。
达斯,s.l.。et al。急性胰腺炎后新诊断糖尿病:一项系统回顾和荟萃分析。肠道63(5), 818-831(2014)。
胰源性糖尿病:治疗的特殊注意事项。Pancreatology11(3), 279-294(2011)。
Kirkegard, J., Cronin-Fenton, D., heidea - jorgensen, U. & Mortensen, F. V.急性胰腺炎与胰腺癌风险:丹麦一项全国性匹配队列研究。胃肠病学154(6), 1729-1736(2018)。
Baena-Diez, j.m.。et al。糖尿病患者病因特异性死亡的风险:一项竞争性风险分析糖尿病护理39(11), 1987-1995(2016)。
阿加瓦尔,S。et al。慢性胰腺炎的自然病程及其进展的预测因素。Pancreatology20.(3), 347-355(2020)。
Nojgaard C。et al。急性胰腺炎到慢性胰腺炎的进展:预后因素、死亡率和自然病程。胰腺40(8), 1195-1200(2011)。
黄天生。et al。慢性胰腺炎与脑血管疾病风险增加相关:台湾一项回顾性人群队列研究医学95(15), e3266(2016)。
Hsu, M. T. Lin, C. L. & Chung, W. S.慢性胰腺炎患者急性冠状动脉综合征风险增加:一项全国性队列分析。医学95(20), e3451(2016)。
汗,D。et al。慢性胰腺炎患者心肌梗死的患病率。胰腺50(1), 99-103(2021)。
Ajjan, R. A。et al。糖尿病的抗血栓治疗:哪种,何时,持续多长时间?欧元。心J。42(23), 2235-2259(2021)。
卡波达诺,D. &血管奥利略,D. J.抗血栓治疗动脉粥样硬化性心血管疾病在冠心病和糖尿病患者风险降低。循环142(22), 2172-2188(2020)。
Griffin, s.j, Leaver, J. K. & Irving, G. J.二甲双胍对心血管疾病的影响:2型糖尿病患者随机试验的荟萃分析。Diabetologia60(9), 1620-1629(2017)。
本杰明,e.j.。et al。心脏病和中风统计数据-2019年更新:美国心脏协会的一份报告。循环139(10), e56-e528(2019)。
资金
作者的研究没有得到任何财政支持。
作者信息
作者及隶属关系
贡献
S.H.L.和K.H.对研究的概念化和设计做出了贡献,并修改了手稿。D.K.J.和J.H.C.进行了正式的分析、调查,并起草了手稿。w.h.p.、j.k.r.和Y.K.对这项工作的调查和解释作出了贡献。所有作者均已阅读并批准最终稿。
相应的作者
道德声明
相互竞争的利益
作者声明没有利益竞争。
额外的信息
出版商的注意
施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.
关于本文
引用本文
张德凯,崔俊华,白伟华et al。糖尿病和急性胰腺炎病史患者心血管疾病和死亡率的风险:一项全国性队列研究Sci代表12, 18730(2022)。https://doi.org/10.1038/s41598-022-21852-7
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s41598-022-21852-7