摘要
本研究的目的是调查心房颤动(AF)的患病率和发生率,并描述入住长期护理医院的患者的临床特征、风险概况、预防中风的抗凝治疗类型和临床结果。我们使用2014年1月1日至2017年10月31日在两家长期护理医院生活的65岁或以上患者的电子医疗记录数据进行了回顾性队列研究。对1148例患者(平均年龄84.1±7.9岁,74.2%为女性)的总体数据进行分析。在基线时,CHA的中位数2DS2-VASc评分为4 (IQR为3-5),has - bleed评分为2 (IQR为2 - 3)。我们观察患者的平均时间为3.7年。2014年1月1日AF点患病率为29.6% (95% CI 25.8 ~ 33.7)。1年累积发病率为4.0%(2.8-5.6)。48%的房颤患者使用口服抗凝药物。TIA、卒中或全体性动脉栓塞综合结局的1年累积发生率分别为0.6%(0.1-3.1)和1.7%(0.5-4.6),出血发生率分别为2.6%(0.9-6.2)和1.8%(0.5-4.8),房颤患者使用口服抗凝药物或不使用口服抗凝药物。在长期护理的医院患者中,我们观察到房颤的高负担。然而,只有大约一半的房颤患者接受口服抗凝治疗以预防中风。
简介
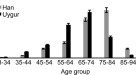
心房颤动(AF)是最常见的心律失常,其发病率随年龄增长而增加1.而房颤在普通人群中的总体患病率为1%至2%1,2,3.,在60至70岁的人群中增加到4%左右,在85岁或以上的人群中达到近20%4.随着预期寿命的增加,未来几十年65岁及以上的老年患者比例将不断增加1.这反过来又会导致房颤患者中风、住院、充血性心力衰竭和死亡风险升高的比例大幅增加5,6,7,8.
目前的指南建议非维生素K拮抗剂口服抗凝剂(NOAC)优于维生素K拮抗剂(VKA)预防非瓣膜性房颤患者的中风9.然而,由于中风和出血的风险增加,平衡口服抗凝剂(OAC)在老年房颤中的有效性和安全性具有挑战性。在老年人群中,OAC的处理可能会因虚弱、多药、肾功能或肝功能受损而进一步复杂化。这些因素可能是导致老年房颤患者使用OAC预防中风的处方率较低的原因。
有很大一部分无法照顾自己的老年人住在养老院和长期护理医院等长期护理设施中。这些机构收治的病人通常年事已高,患有各种并存疾病,因此需要长期护理和医疗。尽管以前的研究评估了老年人群中房颤的患病率和抗凝治疗的管理,但在养老院或长期护理医院的患者中缺乏证据10,11.
因此,本研究的目的是收集流行病学数据,如房颤的患病率和发病率,并描述入住长期护理医院的老年人的临床特征、风险概况、抗凝治疗模式和结局。
方法
研究设计
我们使用两家长期护理医院的电子医疗记录数据进行了回顾性队列研究。维也纳医科大学伦理委员会批准了该研究(EK Nr. 2124/2017),并确认本次回顾性数据分析不需要患者个人同意书。本研究按照相关指南和法规进行。对于这项观察性研究的报告,我们遵循了加强流行病学观察性研究报告(STROBE)的声明12.
研究人口和环境
我们分析了两家长期护理医院(Haus der Barmherzigkeit Tokiostrasse和Haus der Barmherzigkeit Seeboeckgasse,奥地利维也纳)连续收集的老年人数据。这些医院为老年人、多病患者和慢性病患者提供长期护理和专门医疗护理,患者对护理的依赖程度各不相同。我们纳入了65岁及以上的患者,无论所需的护理依赖水平如何,均为2014年1月1日已入院或此后至2017年10月31日新入院的患者(见补充图)。S1).随访结束于2017年10月31日,随访时间最长为3年10个月。
数据源和变量
我们获得了患者特征的数据,包括临床诊断和老年病学评估、用药、实验室结果以及入院日期——如果适用的话——从长期护理医院出院的日期、出院目的地的信息和死亡。根据现有数据,我们计算Charlson共病指数13, CHA2DS2-VASc评分(充血性心力衰竭,高血压,年龄≥75岁,糖尿病,中风或短暂性脑缺血发作[TIA],血管疾病,年龄65 - 74岁,性别分类)评估中风风险14出血风险的has - red评分(高血压、肾/肝功能异常、中风、出血史或易感性、INR不稳定、老年人、药物/酒精伴发)评分15在基线。根据欧洲心脏病学会(ESC)房颤诊断和管理指南,出血高风险定义为has - bleed评分≥3分9.
对于基线和结果变量,我们使用了根据治疗医生指定的国际疾病分类第10版(ICD-10)的诊断代码和/或来自电子病历的免费文本信息的组合。如果某个诊断的ICD-10代码丢失了,我们依靠的是明确报告的自由文本信息。诊断日期与自由文本信息一致/验证。对于2014年1月1日之后新入院的患者,入院后5天内的任何诊断均被视为既往病史。确诊时间以2014年1月1日起或入院至电子病历首次备案时间计算。来自研究团队的有经验的临床医生澄清了与疾病诊断和日期相关的歧义。如有必要,电子病历由人工审阅。
采用解剖治疗化学(ATC)分类方法来鉴别口服抗凝药物(包括利伐沙班、达比加群、阿哌沙班、依多沙班的VKA或NOAC)和其他相关药物(肠外抗凝药物、血小板抑制剂、抗糖尿病药、非甾体抗炎药)。我们认为,如果在2014年1月1日之后的5天内开了药,或者如果在2014年1月至2017年10月入院后的5天内开了药,那么药物就会出现在基线水平。
结果测量
主要结果是房颤的患病率和房颤患者在基线时OAC的比例。次要结局是新生房颤的发生率和TIA、中风或非中枢神经系统(CNS)系统性动脉栓塞的复合因素,以及随访期间的出血和全因死亡。房颤被定义为至少一种诊断为阵发性、持续性或永久性房颤、典型或非典型心房扑动或未指明的房颤和心房扑动(ICD-10代码I48.X)。OAC定义为病历记载的口服抗凝剂处方(VKA或NOAC)。
蒂雅被定义为局灶性神经缺损,在24小时内完全缓解(ICD-10代码G45.X)。中风指任何持续至少24小时的非创伤性局灶性神经功能缺损,包括任何缺血性或出血性卒中(ICD-10编码I61.X-64.X)。非中枢神经系统系统性动脉栓塞定义为任何导致外周动脉急性失血的非脑外周栓塞(ICD-10代码I74.X)。出血包括任何临床上明显的外伤性或非外伤性颅内、胃肠道或其他颅外出血(如眼部、皮肤和软组织、肾脏、腹膜后、心包、关节内)。颅内出血包括硬膜外、硬膜下、蛛网膜下腔或脑内出血。消化道出血被定义为任何临床上发生于上或下消化道的明显出血。对于所有结果变量,我们使用了根据治疗医师分配的ICD-10编码的诊断代码和/或上述电子医疗记录中的免费文本信息的组合。
数据管理
我们从电子病历中检索患者数据,遵循当前的患者数据安全标准。授权研究人员于2018年1月将中心医院管理软件中的数据导出并化名为Microsoft Excel 2016 (Microsoft, Redmond, USA)电子表格。我们获得了2014年1月1日及之后入院的横断面数据。随访结束于2017年10月31日。我们检查了符合条件的患者数据的可信度。
统计分析
对于连续的基线变量,如果数据近似正态分布,我们计算均值和标准差;我们计算了非正态分布数据的中位数、25百分位和75百分位。我们直观地评估数据是否正态分布。我们将分类数据报告为绝对频率和相对频率。2014年1月1日- 2017年1月1日,我们估计患病率,计算95%置信区间作为房颤患者占比(点患病率)。在非正态分布(连续变量)的情况下,采用双侧t检验或Wilcoxon检验和卡方检验(分类变量)对非房颤患者与房颤患者进行比较。
我们计算了从基线到因任何原因死亡、从长期护理医院出院或结束随访的时间。患者在从长期护理医院出院或随访期结束时(2017年10月31日)进行了筛查。用95%置信区间(ci)进行Kaplan-Meier分析来估计死亡率。我们计算了发生(1)自发性房颤,(2)中风,TIA,或全身性动脉栓塞,(3)首次出血,或(4)任何原因死亡的时间。如果没有事件发生,我们计算出院时间或随访结束。对于临床结果,我们分别估计了竞争风险的累积发生率,将任何原因的死亡作为竞争风险(Fine & Gray)。为了确定全因死亡(TIA、中风或全身性栓塞和房颤患者出血的复合因素)的可能危险因素,我们计算了单变量竞争风险回归模型(原因特异性危险模型)。如果单变量模型中的p值小于0.05,则相应的变量进入多变量模型。p值小于0.05被认为有统计学意义。情景应用程序®软件版本9.4 (SAS Institute, Cary, NC, USA)和STATA 14.1版本(StataCorp LP, College Station, TX, USA)用于统计分析。
结果
研究人群
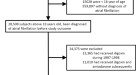
总的来说,我们分析了来自两家长期护理医院的1148名患者的数据。研究流程图(图。1)显示了从2014年1月1日(N = 540)到2017年10月31日(N = 608)的患者选择过程和住院患者数量。中位随访时间为3.7年(四分位范围[IQR] 1.8-3.8)。患者平均年龄84.1±7.9岁;74.2%为女性。我们在表中列出了房颤患者(N = 347)和非房颤患者(N = 801)的基线特征1.与非房颤患者相比,房颤患者有更多的合并症,如高血压、糖尿病、心力衰竭、缺血性和瓣膜性心脏病以及卒中或TIA病史。在伴有和不伴有OAC的AF患者中,我们发现在体重指数(BMI)和has - bleed评分以及恶性肿瘤和出血史方面存在差异(补充表)S1).除抗凝外,没有患者接受左心耳闭塞或其他形式的血栓栓塞预防。
房颤的患病率、风险概况和抗凝治疗
2014年至2017年,相关年份1月1日的患病率在29.6%至32.5%之间2).在研究期间新入院的608例患者中,187例有房颤,转化为期间患病率为30.8% (95% CI 27.1-34.6)。所有房颤患者均有CHA2DS2-VASc评分≥2分,除1名男性患者为1分外。在347例房颤患者中,48.4%(168 / 347)患者使用口服抗凝剂。
新生房颤发生率
在研究期间,801例基线时无房颤的患者中有55例(6.9%)发生了新生房颤。1年、2年和3年的新生房颤累积发病率列于表中3..
临床结果
中风、TIA或全身性动脉栓塞的发生率
1148例患者中42例(3.7%)发生卒中、TIA或全身性动脉栓塞的综合终点。我们观察到32例中风,9例tia和3例全身性动脉栓塞。在竞争风险分析中,在接受OAC的房颤患者中,卒中、TIA或系统性动脉栓塞的累积发生率从1年的0.6上升到3年的3.6%。相比之下,在未接受OAC治疗的房颤患者中,累积发病率从1.7增加到4.5%(见表)3.).在伴有和不伴有OAC的AF患者中,没有发现卒中、TIA或系统性动脉栓塞的风险有显著差异(见表)S2).
出血发生率
35例患者发生36次出血(15例颅内出血,12例消化道出血,9例其他颅外出血)。在竞争性风险分析中,无OAC的AF患者1-、2-和3年累积出血发生率在数字上低于有OAC的患者(见表)3.).在伴有OAC和不伴有OAC的房颤患者中,出血风险无显著差异(见表)S2).
根据补充资料中的AF和OAC,我们提供了卒中、TIA、全体性栓塞或出血复合终点的累积发病曲线(补充图。S2).
全因死亡的风险
在研究期间死亡的602例患者(52.4%)中,196例发生房颤,406例基线时没有房颤。Kaplan-Meier分析显示,伴有OAC的房颤患者1年、2年和3年全因死亡率低于无OAC的房颤患者。2).单因素分析显示,房颤患者的OAC与死亡风险显著降低相关(HR 0.62;95% CI 0.47-0.82, p < 0.001),但在包括年龄、女性性别和BMI在内的多变量回归分析中,没有死亡的独立预测因子(HR 0.77;95% CI 0.56-1.06, p = 0.11;见表S2).
讨论
在这项对长期护理医院收治的老年人的回顾性队列研究中,我们发现房颤的患病率很高2DS2-VASc评分≥2在99%的房颤患者中,≥4在88%的房颤患者中,只有48%的房颤患者接受了OAC。
在我们的研究中,房颤的点患病率在29.6%到32.5%之间。这比之前观察性研究报告的患病率要高。一项来自法国的横断研究发现,10.1%的疗养院居民患有房颤10.同样,美国全国养老院调查报告2004年的患病率为10.9%16.Tulner等人观察到,在日间诊所就诊的老年门诊患者中,患病率为20.1%11.这些与我们发现的差异可能是由研究人群和环境的差异所解释的。虽然我们研究中患者的平均年龄相似,但他们都有各种既往病史和危险因素。本研究中的患者入住了一家长期护理医院,该医院为患者提供各种医疗保健设施和比养老院更大程度上的永久性医疗护理。因此,这些患者往往比非医疗疗养院的患者病情更重,房颤发生率更高。此外,在长期护理医院进行定期体检可能会提高房颤的检出率。
尽管除1例AF患者外,所有患者的OAC推荐等级均为IA级17在美国,只有一半人收到了。相比之下,接受低分子肝素(16%)和血小板抑制剂(27%)的患者比例较小。尽管这些都是预防房颤患者中风的非标准疗法,但患者接受这些治疗可能是为了预防中风以外的适应症。先前的研究还发现,尽管中风风险增加,但房颤患者中有很大比例没有接受OAC18.一项来自美国的大型横断面研究发现,47.8%的房颤疗养院居民接受了OAC19.同样,Bahri等人报道,在法国,有49.1%的房颤疗养院居民接受了抗凝剂10.一项系统综述发现,长期护理房颤患者接受华法林治疗的比例从17%到57%不等20..
根据法国一项针对照顾养老院居民的医生的调查,不开抗凝剂处方的主要原因是反复摔倒、认知障碍和高龄10.在年龄和CHA方面,本研究的患者特征似乎与我们的研究相似2DS2-VASc得分。因此,在我们的队列研究中,这些因素也可能是不给房颤患者开OAC的原因。此外,现有的风险预测工具没有反映出血的风险和基础疾病的预后可能影响了OAC的决定。尽管在我们的研究中47%的患者has - bleed评分≥3,但伴有OAC的房颤患者的出血风险似乎并不比没有OAC的患者高。
尽管CHA很高2DS2-VASc评分时,我们观察到AF和OAC患者中TIA、卒中或全体性栓塞事件的发生率较低(1.9 / 100人-年),而无OAC(3.5 / 100人-年)。一项对德国健康索赔数据库的分析发现,75岁或以上因房颤而接受OAC的患者具有相似的平均CHA,其中风或全身性栓塞的发生率相似,为1.8 / 100人-年2DS2-VASc得分21.然而,结果的定义是不同的。在我们的队列研究中,没有OAC的患者中TIA、卒中或全身性栓塞事件的发生率较低,可能是由于使用低分子肝素所致。由于肾功能受损,即使是预防剂量也足以用于治疗性抗凝。在我们的研究人群中,随访期间中风和全身性栓塞发生率较低的另一个解释可能是对CHA中未体现的其他可改变的危险因素和共病的优化管理2DS2-VASc得分。
尽管在基线时房颤的患病率很高,但我们在随访中观察到房颤的发病率很高。这很可能是由于本研究中高水平的医疗关注导致的高检出率,这意味着在这种情况下,医生不应避免对房颤进行长期监测。
与房颤和无房颤的患者相比,OAC与房颤患者较低的死亡率相关。尽管如此,OAC已经证明了其降低死亡率的潜力22,这种好处通常是由血栓栓塞事件的减少所驱动的。在我们的研究中,OAC是死亡率的独立预测因子;然而,一旦将其他预后因素纳入多变量分析,OAC与死亡率的差异并不相关。因此,在我们的老年人口中观察到的死亡率下降很可能不是由OAC本身引起的,而是可以用测量和未测量的混杂因素来解释。与较高发病率和死亡率相关的患者特征可能有助于某些房颤患者避免发生OAC。
我们的研究有几个局限性。首先,我们进行了一项基于电子病历的回顾性研究,并附加了易受不同类型偏见影响的选择性手工病历审查。我们可能遗漏或错误分类了基线诊断和结果诊断的相关信息。我们不能根据常见的出血定义对出血进行分类,例如根据出血学术研究协会(BARC)和国际血栓与止血学会(ISTH),因为不是所有的出血成分都被常规收集。但是,我们认为大部分病历中提到的出血都具有足够的临床意义,可以归类为大出血。在将我们的出血率与其他研究报告进行比较时,必须考虑到这一点。其次,研究人群包括来自两家长期护理老年医学机构的患者。因此,本研究的结果不能外推到其他老年环境,如社区、疗养院或急症护理医院。第三,我们无法获得更多的信息,为什么医生决定支持或反对OAC,或基于个人患者的特征或偏好减少使用OAC的剂量。因此,我们无法探索导致医生决定完全不开OAC或减少处方剂量的因素可能产生的混淆效应,也无法探究该决定是否合理或定期复查。 Forth, patients with AF receiving low-molecular-weight heparin instead of OAC might confound our results regarding clinical outcomes. Finally, results from regression analysis of this cohort study should be interpretated with caution. Due to the low number of stroke, TIA, systemic arterial embolism, and bleeding events, we might have missed a significant influence of OAC on these events in our analyses.
在长期护理的医院患者中,我们观察到房颤的高患病率。然而,尽管有明确的适应证,只有大约一半的房颤患者接受了OAC预防中风。为了理解我们发现的潜在原因,需要对长期护理医院住院患者进行大型前瞻性多中心研究。这可能有助于进一步优化和个性化预防老年房颤的中风和出血。
数据可用性
本研究中分析的数据集可根据合理要求从通讯作者处获得。
参考文献
加油,a.s.。et al。成人房颤的患病率:节律管理和中风预防的国家意义:房颤(ATRIA)研究中的抗凝和危险因素。《美国医学会杂志》285, 2370-2375(2001)。
Feinberg, W. M, Blackshear, J. L, Laupacis, A., Kronmal, R. & Hart, R. G.心房颤动患者的患病率、年龄分布和性别。分析与启示。拱门。实习生。地中海。155, 469-473(1995)。
Naccarelli, g.v, Varker, H, Lin, J. & Schulman, K. L.美国心房纤颤和扑动患病率的增加。点。j .心功能杂志。104, 1534 - 1539。https://doi.org/10.1016/j.amjcard.2009.07.022(2009)。
Heeringa, J。et al。心房颤动的患病率、发病率和终生风险:鹿特丹研究。欧元。心J。27, 949 - 953。https://doi.org/10.1093/eurheartj/ehi825(2006)。
Wolf, P. A., Abbott, R. D. & Kannel, W. B.心房颤动作为卒中的独立危险因素:Framingham研究。中风22, 983-988(1991)。
新泽西州帕特尔。et al。2000 - 2010年美国房颤住院的当代趋势:对医疗计划的影响循环129, 2371 - 2379。https://doi.org/10.1161/circulationaha.114.008201(2014)。
本杰明。et al。心房颤动对死亡风险的影响:弗雷明汉心脏研究循环98, 946 - 952。https://doi.org/10.1161/01.cir.98.10.946(1998)。
王铁杰;et al。心房颤动和充血性心力衰竭的时间关系及其对死亡率的联合影响:弗雷明汉心脏研究循环107, 2920 - 2925。https://doi.org/10.1161/01.Cir.0000072767.89944.6e(2003)。
Hindricks G。et al。与欧洲心胸外科协会(EACTS)合作制定的2020 ESC房颤诊断和管理指南。欧元。心J。42, 373 - 498。https://doi.org/10.1093/eurheartj/ehaa612(2021)。
Bahri, O。et al。法国某疗养院房颤患者口服抗凝药使用不足:住院医师特征和医生态度的比较。j。Geriatr。Soc。63, 71 - 76。https://doi.org/10.1111/jgs.13200(2015)。
塔尔纳(Tulner)。et al。虚弱老年门诊房颤患者口服抗凝剂治疗不足的原因:一项前瞻性描述性研究。药物老化27, 39-50。https://doi.org/10.2165/11319540-000000000-00000(2010)。
von Elm, E。et al。加强流行病学观察性研究报告(STROBE)声明:报告观察性研究的指南。流行病学18, 800 - 804。https://doi.org/10.1097/EDE.0b013e3181577654(2007)。
Charlson, m.e, Pompei, P, Ales, K. L. & MacKenzie, c.r.纵向研究中预后共病分类的新方法:发展和验证。J.慢性疾病40, 373 - 383。https://doi.org/10.1016/0021 - 9681 (87) 90171 - 8(1987)。
Lip, G. Y., Nieuwlaat, R., Pisters, R., Lane, D. a . & Crijns, H. J.使用一种新的基于风险因素的方法来预测心房颤动中中风和血栓栓塞的临床风险分层:心房颤动的欧洲心脏调查。胸部137, 263 - 272。https://doi.org/10.1378/chest.09-1584(2010)。
高压球阀,R。et al。一种新颖的用户友好评分(has - bleed)用于评估心房颤动患者1年大出血的风险:欧洲心脏调查。胸部138, 1093 - 1100。https://doi.org/10.1378/chest.10-0134(2010)。
Reardon, G., Nelson, W. W., Patel, A. A., Philpot, T. & Neidecker, M.美国疗养院房颤患病率:1985-2004年全国疗养院调查结果。j。地中海,Dir。Assoc。13, 529 - 534。https://doi.org/10.1016/j.jamda.2012.03.007(2012)。
Kirchhof, P。et al。与EACTS合作制定的2016 ESC房颤管理指南。欧元。心J。37, 2893 - 2962。https://doi.org/10.1093/eurheartj/ehw210(2016)。
Ohlmeier, C, Mikolajczyk, R, Haverkamp, W. & Garbe, E.德国老年人心房颤动的发生率、患病率和抗血栓治疗。EP Europace15, 1436 - 1444。https://doi.org/10.1093/europace/eut048(2013)。
Alcusky, M。et al。2011年至2016年美国心房颤动疗养院居民抗凝剂使用的变化。j。心脏协会。8, e012023。https://doi.org/10.1161/jaha.119.012023(2019)。
Neidecker, M., Patel, A. A., Nelson, W. W. & Reardon, G.长期护理中华法林的使用:一项系统综述。BMC Geriatr。12, 14-14。https://doi.org/10.1186/1471-2318-12-14(2012)。
Hohmann C。et al。非维生素K口服抗凝药与phenprooumon在老年和非老年非瓣膜性心房颤动患者中的比较。Thromb。Haemost。119, 971 - 980。https://doi.org/10.1055/s-0039-1683422(2019)。
Arbel, R。et al。直接口服抗凝与中高危心房颤动的死亡率。心105, 1487年。https://doi.org/10.1136/heartjnl-2018-314476(2019)。
资金
奥地利维也纳维也纳医科大学第一医学系获得了辉瑞奥地利公司的无限制赠款。
作者信息
作者和隶属关系
贡献
概念和设计:c.a., c.g., g.o., m.s., G.W.数据采集:g.o., G.W.数据分析和/或数据解释:c.a., g.g., d.m., s.n., i.p., m.s., G.W.起草稿件:GW。修改手稿:C.A。,G.G C.G。d.m., S.N, G.O I.P,硕士
相应的作者
道德声明
相互竞争的利益
CG、GG、DM、SN、GO和GW没有利益冲突。CA因演讲和参与拜耳、BMS/辉瑞和第一三共的顾问委员会而获得酬金。IP因演讲和参与拜耳、辉瑞和第一三共的顾问委员会而获得酬金。微软获得了礼来、诺华、辉瑞、安进、赛诺菲-安万特、罗氏和勃林格的酬金。
额外的信息
出版商的注意
施普林格自然对出版的地图和机构附属的管辖权要求保持中立。
补充信息
权利与权限
开放获取本文遵循创作共用署名4.0国际许可协议(Creative Commons Attribution 4.0 International License),该协议允许在任何媒体或格式中使用、分享、改编、分发和复制,只要您给予原作者和来源适当的署名,提供创作共用许可协议的链接,并说明是否有更改。本文中的图片或其他第三方材料包含在文章的创作共用许可中,除非在材料的信用额度中另有说明。如果材料不包含在文章的创作共用许可中,并且您的预期用途不被法律法规允许或超出了允许的用途,您将需要直接从版权所有者那里获得许可。欲查看此许可证的副本,请访问http://creativecommons.org/licenses/by/4.0/.
关于本文
引用本文
G.瓦格纳,M.斯米卡尔,C.吉辛格。et al。两家长期护理医院老年房颤患者的流行病学、风险概况、管理和结局Sci代表12, 18725(2022)。https://doi.org/10.1038/s41598-022-22013-6
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s41598-022-22013-6