摘要
我们的目的是确定Hounsfield单位(HU)相关变量与经皮肾镜取石术(PCNL)结果之间的关系。我们招募了2014年1月至2019年10月期间接受单路PCNL的单肾结石(1-3 cm)患者。对人口统计学和结石特征进行回顾性分析。术前计算机断层扫描(CT)和PCNL后至少3个月内的随访CT纳入本分析。无结石状态定义为术后3个月内残留结石≤2mm。使用自由拉伸技术测量HU和横截面积(CSA)。我们使用逻辑回归模型对结果进行了hu相关变量的分析。总共683例患者中有188例符合纳入标准。无结石率(SFR)为79.2%。无结石组和残余组在年龄、性别、BMI、ASA分级、侧边性、术前冲击波碎石、结石大小、结石负荷、皮肤-结石距离和HU方面无显著差异。 CSA and HU/CSA in the stone-free and remnant groups were 94.5 ± 46.1 and 128.3 ± 98.5 (p = 0.043) and 10.1 ± 5.6 and 7.3 ± 3.4 (p = 0.001), respectively. Multivariate logistic regression analysis revealed that pelvis, ureteropelvic junction stones, and HU/CSA were independent predictors of SFR. HU did not affect PCNL outcomes. We believe that HU/CSA could be used for determining stone treatment plans and predicting outcomes.
介绍
非对比计算机断层扫描(NCCT)被广泛接受用于诊断尿石症。其灵敏度(> 94%)和特异性(> 95%)均高于x线平片、超声和静脉肾盂造影1。NCCT获得的信息包括结石大小、多样性、位置、解剖异常、皮肤到结石的距离、结石密度(Hounsfield单位[HU])和易碎性(结石异质性指数[SHI]和变异系数[VCSD])。2,3.,4,5。结石的大小对预测自然排尿的可能性很重要。HU, SHI和VCSD与岩石成分和脆性有关,它们决定了冲击波碎石术(SWL)的成功。然而,关于HU在经皮肾镜取石术(PCNL)预后中的预测作用的研究文献很少。6,7,8,9。
用于预测PCNL结果的结石评分系统有stone、CROES肾结石测量图和Guy 's结石评分10,11,12。这些评分系统是根据结石数量、HU、负担、位置、解剖异常和外科医生的经验提出的。在这些评分系统中,只有STONE评分系统包含HU;然而,在该评分系统中,将HU(950)作为临界值的临床证据不足。
本研究旨在确定hu相关变量与PCNL预后之间的关系。我们引入了基于HU和截面积(CSA)的结石密度概念,作为PCNL预后的可能预测因子。
材料与方法
伦理批准
本研究已获得韩国天主教大学机构审查委员会批准(批准号KC18RESI0836)。在涉及人类参与者的研究中执行的所有程序都符合机构和/或国家研究委员会的道德标准以及1964年《赫尔辛基宣言》及其后来的修正案或类似的道德标准。所有用于统计分析的信息都是匿名的,并且韩国天主教大学机构审查委员会放弃了获得知情同意的要求。
患者选择和研究设计
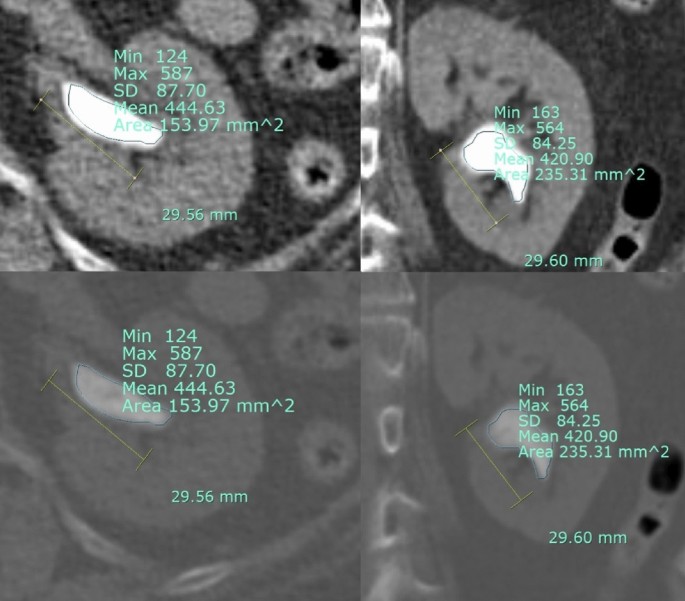
我们回顾性回顾了2014年1月至2019年10月在一所高等教育机构连续接受PCNL的683例患者的数据。总的来说,188例单道PCNL患者,最大结石直径为10 - 30mm,并通过术前和术后CT扫描进行评估。我们的研究分析了hu相关变量对PNL的影响,因此,通常已知对成功率有重大影响的结石大小仅限于10-30-mm大小的单个结石。下花萼中10 - 20毫米大小的石头根据石头管理指南被包括在内13。我们回顾性地评估了患者的特征、NCCT测量的结石相关变量和手术参数(手术时间、结石清除率、血红蛋白、红细胞压积、肌酐、住院时间和并发症)。与结石相关的变量为结石直径、结石位置[输尿管肾盂连接处(UPJ)、肾盂、下/中/上花萼]、结石最大CSA、皮肤-结石距离、最大CSA处自由绘制法HU值、HU标准差SHI。在轴位和冠状位视图中,在植骨视图中设置较大的CSA作为参考值。自由绘制方法是很容易地使用PACS程序,利用数字徒手卡尺(图1)。1)。此外,它是通过在最大CSA下,用自由的手沿着石头形状的内层直接铺设来测量的。两名泌尿科医生,包括一名泌尿科住院医师,评估结石状态并进行结石测量和计算。
我们将无结石状态(SFS)定义为没有残留碎片或临床上不明显的残余结石(≤2mm)。OP时间定义为从经皮穿刺到切口部位最终敷料的时间。
pcnl后的预后数据回顾性收集电子病历。所有患者均进行了术前和术后肾、输尿管和膀胱(KUB)放射学评估和NCCT检查。所有接受PCNL的患者在术后3个月内通过KUB平片和NCCT进行评估。所有病例在术后1周、4-8周和3-6个月进行分析。在常规随访的基础上,每6个月对结石残留患者进行随访。
所有手术均由经验丰富的内分泌科医生完成,他在一年内完成了150多例PCNL。本研究的排除标准是同时双侧PCNL和需要两个以上肾镜束的多重入路。比较SFS患者和残余状态患者的围手术期变量和基线人口统计学。术前数据包括体重指数、美国麻醉学会分类、术前SWL(表1)1)。我们也回顾了手术资料和并发症资料。根据改良的Clavien并发症报告系统记录并发症14。主要终点是计算hu相关变量与PCNL结果之间的相关性。
手术技术
术前对所有患者进行尿液分析和培养,并根据结果给予预防性抗生素治疗。
在全身麻醉下,患者在膀胱镜输尿管置管后采用俯卧位。输尿管置管后置入Foley导尿管。在俯卧位前,将其与输尿管导管一起放入无菌袋中,以防止脱位和污染。术后第1天拔除Foley导尿管。经皮通道采用透视引导穿刺,球囊扩张至24fr。手术中使用20fr肾镜。使用气动和超声波设备(Swiss Lithoclast, EMS Electro Medical System, Switzerland)粉碎石头。完成PCNL后,仔细检查收集系统,并进行肾造影以排除残余结石。除非有任何术中事件或疑似残留结石,否则手术结束时无肾造瘘管插入。除非有UPJ水肿、疑似残留结石或术中明显出血,否则不常规植入D-J15。
统计分析
连续变量以mean±SD或range报告,并使用独立样本Student’s进行比较t-test或Mann-Whitney U test视情况而定。使用卡方或线性逐线性关联检验对分类变量进行统计学显著性分析。我们使用G*Power 3.1 Window程序计算,逻辑回归所需样本数量至少为158个(α误差0.05,Power 1 - β = 0.80, Odds Ratio (OR) = 0.6, Pr(Y = 1 | X = 1)H0 = 0.3),使得本研究的受试者数量足以获得Power。我们使用逻辑回归模型进行单变量和多变量评估,以确定SFS和OP时间的预测因子。p-值< 0.05认为有统计学意义。用类内相关系数(ICC)评估观察者间信度。16。统计分析使用R软件(版本3.3.2,R Foundation for Statistical Computing, Vienna, Austria;http://r-project.org)。G power 3.1 for window。
结果
患者人口统计、结石特征和围手术期数据
2014年1月至2019年10月,683例患者接受了PCNL。随后,495颗因结石数量、大小和道数被排除在外。最终,188例患者符合纳入标准。PCNL术后SFS率为79.2%(149/188),残差率为20.8%(39/188)。比较无结石组和残余组的人口统计学、手术因素和结石特征(表2)1,2);下花萼结石(25.5%比48.7%,p = 0.009)、骨盆和UPJ结石(62.4%比33.3%,p = 0.002)、结石CSA(94.5±46.1比128.3±98.5,p = 0.043)、HU/CSA(10.1±5.6比7.3±3.4,p = 0.001)、手术时间(56.4±22.6比6.55±22.9,p = 0.027)差异均有统计学意义。并发症分类采用改良的Clavien-Dindo分类法(表1)3.)。25例(13.3%)患者共发生31例并发症。
SFR的多因素logistic回归分析
在单因素分析中,以下因素与残留状态显著相关:下花萼结石(p = 0.006,优势比= 2.77)、骨盆或UPJ结石(p = 0.002,优势比= 0.30)、结石CSA (p = 0.013,优势比= 2.77)、HU/CSA (p = 0.00,优势比= 0.87)。在多元logistic回归分析的最终模型中,骨盆和UPJ结石(p = 0.003,优势比= 0.65)和HU/CSA (p = 0.027,优势比= 0.90)是整体患者SFS的独立显著预测因子(表1)4)。下萼石、SSD、HU、SHI、Radio-opacity对SFS无影响。结石状态预测logistic回归模型显著(x2 = 22.497, p = 0.001), Nagelkerke决定系数(R2)的解释能力为48.7%。
讨论
在本研究中,我们重点研究了hu相关变量与CT测量的PCNL结果之间的关系。主要研究结果如下:影响单结石PCNL SFR的因素为结石位置和HU/CSA;影响手术时间的因素是CSA。
对于HU与PCNL预后之间的关系,guucuk等。6,9报告HU的临界值应为677.5,HU值越低,成功率越低。同时,Alper等人。7提示HU、成功率和手术时间之间没有相关性,且当HU值高时,透视时间延长。唯一的大规模研究是CROES集团在2013年采用多中心设计进行的;作者报告说,非常低和高密度的结石成功率下降,需要更长的手术时间8。因此,关于HU对PCNL结果的影响尚无共识。不一致的主要原因是由于测量HU的方法不同,缺乏观察者间的可靠性和可重复性。
在本研究中,影响结石游离率的部位是肾盂;这些石头在盖伊的石头评分系统中被评为I级。使用HU/CSA作为PCNL预后的预测因子,我们证明了具有高HU/CSA值的结石具有高无结石率的趋势。这可以用以下事实来解释:在相同的CSA中,SFR会随着HU的增加而升高,而在相同的HU中,SFR会随着CSA的减少而升高。
在CROES研究中8在极低密度和高密度结石中,PCNL的成功率较低。首先,该研究没有在大量中心采用一致的测量方法。其次,由于CT层厚度和能量方案的差异,在结石评估方面存在异质性。第三,HU倾向于与石材的大小成比例增加17随HU的增大,射电不透明比例增大。综上所述,认为HU本身对OP时间的影响是显著的还不够。在我们的研究中,基于HU、放射不透明度和结石异质性指数的OP时间分析没有显著差异。此外,作为连续变量,OP时间与HU之间无显著相关。
考虑到石头尺寸测量,Patel等人提出了关于限制的问题,因为现有的人工测量存在高度的观察者之间的可变性,以及使用商业化计算机程序的石头测量方法的有效性18,19。然而,没有足够的临床或成本相关的证据开始在临床实践中使用它。另一方面,关于我们使用的自由绘制测量,Tanaka等人。20.建议使用石头CSA测量并使用它来预测SWL结果的效率。
在HU测量的标准化方面,Narayan等。21比较兴趣区域测量技术。对于哪种测量技术是有效的,似乎没有达成共识。莫特利等人。22Nakada等人。23HU和结石直径比是预测钙结石和尿酸结石预后的重要因素。据我们所知,本研究首次报道了HU和CSA的比例及其对PCNL预后的影响。
由于没有标准的测量方法,我们的自由绘制技术可以在几乎所有的PACS程序中用作单一测量。此外,我们将研究人群限制在大于CT厚度大小的单个结石中,并尽量减少部分体积效应。该数据集的同质性代表了本研究的一个优势。
尽管有这些优点,我们的研究也有一些局限性。首先,该研究采用回顾性设计,患者数量较少。虽然结石范围(1.0-3.0 cm)使该组具有异质性,但可以认为偏差最小化,因为它针对的是单结石和单通道PCNL患者。最近,随着为患者提供“自主选择”手术的趋势日益增长,重要的是要注意,对于结石小于2厘米的患者,有可能提供柔性输尿管镜检查,甚至是SWL和柔性输尿管镜检查的“联合方法”24。其次,CSA/HU比率作为预测因子可能是一个混杂变量。因为溶血性尿毒随结石大小的增加而增加25,单独的CSA可能是决定SFR的因素。此外,使用自由抽取结石测量方法的医生之间可能存在测量偏差。然而,在测量Hounsfield单位时,众所周知,无论采用何种测量方法,观察者之间/内部的可变性都显示出很高的一致性概率26,我们的数据在类内相关系数分析中也显示出一致。然而,最大结石直径、CSA和HU不是SFR的显著预测因素,我们使用多变量logistic回归最小化了混杂变量的可能性。影响PCNL预后的变量很多,我们的研究组仅包含单结石和单路PCNL患者。最后,我们没有包括对石头成分的分析。由于这些原因,需要对更大的数字进行前瞻性研究,包括对石头成分的分析。
总之,HU本身对PCNL的预后没有影响。然而,一个与HU相关的变量HU/mm2,可预测SFR。我们认为HU/CSA可用于设计结石治疗方案和预测PCNL的预后。在未来的研究中,HU/CSA可以作为决定输尿管镜手术和SWL预后的有效变量。
数据可用性
在当前研究过程中产生和/或分析的数据集可根据通讯作者的合理要求提供。
参考文献
Smith, R. C, Verga, M., McCarthy, S.和Rosenfield, A. T.急性腰痛的诊断:非增强螺旋CT的价值。学杂志。j . Roentgenol。166, 97-101(1996)。
guucuk, A. & Uyeturk, U. hounsfield单位和密度在尿路结石评估和治疗中的作用。世界J.尼弗罗尔。3., 282-286(2014)。
李俊英。et al。结石异质性指数作为霍斯菲尔德单位的标准偏差:输尿管结石冲击波碎石治疗结果的新预测指标。科学。代表。6, 23988年。https://doi.org/10.1038/srep23988(2016)。
山下先生,S。et al。结石密度变异系数:预测体外冲击波碎石治疗结果的新方法。j . Endourol。31, 384-390(2017)。
Waqas, M., Saqib, I. U, Jamil, M. I, Khan, M. A.和Akhter, S.评估不同计算机断层扫描因素在预测体外冲击波碎石治疗肾结石结果中的重要性。Investig。中国。Urol。59, 25-31(2018)。
Gucuk,。et al。计算机断层扫描确定的Hounsfield单位值能否预测经皮肾镜取石术的结果?j . Endourol。26, 792-796(2012)。
完全懂得,一个。et al。非对比ct计算的hounsfield单位值及其对经皮肾镜取石效果的影响。尿石病。43, 277-281(2015)。
Anastasiadis,。et al。肾结石密度对经皮肾镜取石术(PCNL)结果的影响:泌尿系统学会临床研究室(CROES) PCNL全球研究数据库的分析。Scand。j . Urol。47, 509-514(2013)。
Gucuk, A, Yilmaz, B, Gucuk, S. & Uyeturk, U.对于小于2cm的肾结石,结石的密度和位置是否可以作为决定泌尿外科手术技术的有用参数?一项前瞻性随机对照试验。Urol。J。16中文信息学报,236-241(2019)。
Okhunov, Z。et al。S.T.O.N.E.肾结石测定仪:肾结石新的外科分类系统。泌尿外科81, 1154-1159(2013)。
史密斯,一个。et al。预测经皮肾镜取石术治疗成功的肾结石测量图。j . Urol。190, 149-156(2013)。
Thomas, K, Smith, N. C., Hegarty, N.和Glass, J. M. The Guy 's stone评分:经皮肾镜取石术的复杂性。泌尿外科78, 277-281(2011)。
土耳其人,C。et al。尿石症的诊断和保守治疗指南。欧元。Urol。69, 468-474(2016)。
J. J.德拉罗塞特。et al。经皮肾镜取石术并发症的分类及Clavien评分的验证。欧元。Urol。62(2), 246-255(2012)。
蔡绍文。et al。完全无管与标准经皮肾镜取石术治疗肾结石:临床结果和成本分析。j . Endourol。28, 1487-1494(2014)。
顾天坤,李明英,李明英。信度研究中类内相关系数的选择与报告准则。j . Chiropr。地中海。15, 155-163(2016)。
斯图尔特,G。et al。结石大小限制了霍斯菲尔德单位用于预测草酸钙结石成分的使用。泌尿外科85, 92-95(2015)。
帕特尔,s.r。et al。通过非对比计算机断层扫描自动测量肾结石体积比手工线性测量更具有可重复性。j . Urol。186中文信息学报,2275-2279(2011)。
山下先生,S。et al。三维平均结石密度测量是预测体外冲击波碎石成功的最佳方法。Int。j . Urol。26, 185-191(2019)。
田中,M。et al。计算机断层扫描上的结石衰减值和截面积可预测冲击波碎石术的成功。韩国j·乌罗尔54, 454-459(2013)。
纳拉扬,v.m.。et al。评价感兴趣区域测量策略在计算机断层扫描上表征上尿路结石。j . Urol。197, 715-722(2017)。
Motley, G., Dalrymple, N., Keesling, C., Fischer, J. & Harmon, W. Hounsfield单位密度在尿路结石成分测定中的应用。泌尿外科58, 170-173(2001)。
中田,s.y。et al。临床用非对比螺旋计算机断层扫描测定结石成分。泌尿外科55, 816-819(2000)。
Inoue, T., Okada, S., Hamamoto, S.和Fujisawa, M.逆行肾内手术:过去,现在和未来。Investig。中国。Urol。62, 121-135(2021)。
小j·c·威廉姆斯et al。宽束准直螺旋CT衰减值校正:尿路结石体外试验。专科学校Radiol。8, 478-483(2001)。
G. W. Disselhorst。et al。非增强计算机断层扫描测量尿石密度的观察者间和观察者内一致。j . Endourol。34中文信息学报,417-422(2020)。
资金
本研究由韩国天主教大学首尔圣母医院研究基金资助。
作者信息
作者及单位
贡献
h.w.m.:稿件撰写、统计、项目开发;硕士:稿件编辑;y.h.p.:项目开发、稿件编辑、数据收集;w.j.b.:稿件编辑和项目开发;U-S.H。:manuscript editing and project development; S-H.H.: project development; J.Y.L.: project development; S.W.K.: project development; H.J.C.: project development, data collection, and statistics. All authors reviewed the manuscript.
相应的作者
道德声明
相互竞争的利益
作者声明没有利益冲突。
额外的信息
出版商的注意
b施普林格《自然》杂志对已出版的地图和机构的管辖权要求保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,该协议允许以任何媒介或格式使用、共享、改编、分发和复制,只要您适当地注明原作者和来源,提供知识共享许可协议的链接,并注明是否进行了更改。本文中的图像或其他第三方材料包含在文章的知识共享许可协议中,除非在材料的署名中另有说明。如果材料未包含在文章的知识共享许可中,并且您的预期用途不被法律法规允许或超过允许的用途,您将需要直接获得版权所有者的许可。如欲查阅本许可证副本,请浏览http://creativecommons.org/licenses/by/4.0/。
关于本文
引用本文
Moon, h.w., Taeyb, M., Park, Y.H.et al。霍斯菲尔德单位相关变量对经皮肾镜取石术结果的影响。Sci代表12, 18451(2022)。https://doi.org/10.1038/s41598-022-23383-7
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s41598-022-23383-7