插画:Kasia Bojanowska
2016年,药理学家苏珊·豪利特写了一篇关于怀孕期间激素水平如何影响心脏功能的研究,并把它寄给了一家杂志。
当审稿人的评论回来时,其中两人提出了一个意想不到的问题:雄性小鼠的组织在哪里?
加拿大哈利法克斯达尔豪西大学的豪利特和她的团队在研究与怀孕有关的高激素水平时,只使用了雌性动物。“我真的很惊讶,他们想让我们在男性身上重复所有的事情,”她说。
尽管如此,他们还是照办了,他们的研究结果于2017年发表。不出所料,他们发现激素黄体酮对男性心脏功能没有影响;在女性中,它影响心脏细胞的活性1.
对于增加男性的要求,豪利特的心情很复杂。“这是一个很大的要求,需要进行更多的研究。”但总的来说,她补充说,在研究中考虑性别因素非常重要。“我非常支持在男性和女性身上都做实验。”
许多科学的把关人——资助机构和学术期刊——也有同样的感觉。在过去十年左右的时间里,越来越多的资助者和出版商,包括美国国立卫生研究院(NIH)和欧盟,一直要求研究人员在他们的细胞和动物模型研究中考虑两性。
推动这些政策的主要因素有两个。其中之一是人们越来越认识到,基于性别的差异,通常与激素特征或性染色体上的基因有关,可以影响对药物和其他治疗的反应。另一个是认识到包括两性可以增加科学探索的严谨性,提高可重复性,并为科学追求开辟问题。
当研究确实包括两性时,结果可能对健康很重要。例如,众所周知,性会影响人们对常见药物的反应,包括一些抗生素2女性的血压比男性低时,患心血管疾病的风险似乎就会上升3..
COVID-19提供了另一个关于为什么应该考虑性的现成例子。更多的人死于这种疾病4而女性似乎更容易受到被称为长冠状病毒的一系列挥之不去的症状的影响5.
为什么男女对疼痛的感觉不同
荷兰奈梅亨大学医学中心(Radboud University Medical Center in Nijmegen)的性别医学专家Sabine Oertelt-Prigione说,研究不止一种性别的最大优势是“你可能会发现其他方法找不到的潜在途径、解决方案或新问题”。
但是,重现性和严谨性方面所希望的改进迟迟未能实现。这些政策在何时以及如何将不同性别纳入研究设计的问题上引发了相当大的困惑和争议,一些研究人员认为,目前对“性别”的定义过于二元化和生硬。
位于马里兰州贝塞斯达的美国国立卫生研究院女性健康研究办公室(ORWH)主任珍妮·克莱顿(Janine Clayton)在电子邮件评论中说:“接受性研究重要性的科学家越来越多。自然.“不过,还有改进的空间。”
减少表示
随着越来越多的女性在二十世纪中后期进入研究领域,她们中的一些人开始注意到许多临床研究忽视了两性。
缺乏女性参与者的部分原因是对一场悲剧的反应:在怀孕期间使用一种名为沙利度胺的镇静剂被发现会导致先天性异常。结果之一是,1977年美国食品和药物管理局(FDA)建议几乎所有可能怀孕的女性都被排除在早期临床试验之外——这些试验是在健康志愿者身上测试疗法的安全性和有效性。一项旨在保护女性的政策最终却留下了关于药物如何影响女性的信息真空。
研究人员和资助者开始意识到,将很大一部分人口排除在这些研究之外,或将性别混合进行分析,将产生临床后果。作为回应,NIH于1990年建立了ORWH,并在三年后开始要求将女性纳入临床研究。

萨力多胺导致数千名婴儿(现在已经成年)出现先天性异常,这些婴儿的母亲在怀孕期间服用了这种药物。为了应对这一悲剧,女性通常被排除在临床试验之外。图源:贡萨洛·阿罗约·莫雷诺/盖蒂
然而,直到最近,在基础科学中,性才被边缘化。十几年前,资助者和出版商开始解决这种不平衡的问题。2010年,加拿大卫生研究所实施了一项要求,要求纳入性别和性别分析;2013年,欧盟推出了类似的指导方针,并将其加强为2020年的授权。2016年,也就是豪利特的团队被要求在他们的工作中加入第二性别的那一年,美国国立卫生研究院颁布了一项政策,要求在涉及细胞、组织和动物的研究中纳入两种性别,部分原因是为了在任何临床研究完成之前就发现性别效应的信号。
出版界也在推动类似的透明度。2016年,它发布了《研究中的性别与性别平等》(SAGER)指南,规定了如何在已发表的研究中报告基于性别的差异。个别出版商,包括施普林格自然(发布自然),它们都有自己的政策,鼓励研究人员按性别(定义为一系列生物学特征)报告结果,有时也按性别(社会定义)报告结果。
即使走到这一步也不容易。自2012年以来,克莱顿一直是ORWH解释“性别作为生物变量”(SABV)的先锋。加州斯坦福大学科学史专家朗达·希宾格(Londa Schiebinger)密切参与了这项工作,他说:“我每年都看着她和其他人经历这些事情。”“仅仅是为了让性作为一个生物变量通过这些研究所,她就必须去这些(NIH)研究所,为自己的观点辩护。”
根据克莱顿的说法,美国国立卫生研究院的SABV政策的期望是,研究人员寻找性别或性别差异的影响,或者为研究单一性别提供明确的理由。“寻找性别或性别差异的影响,”克莱顿写道,“是一个机会,而不是障碍。”
但即使这项政策已经推出,一些研究人员仍认为是后者。
性的复杂性
在动物和细胞研究中解释性别并不像听起来那么简单。
在解剖学等广泛指标的基础上描述性别,忽略了激素的更深层次的复杂性,而激素是许多已确定或潜在的男性和女性差异的关键因素。纽约冷泉港实验室(Cold Spring Harbor Laboratory)的分子生物学家杰西卡•托尔库恩(Jessica Tollkuhn)说,没有接受过内分泌科训练的人“可能不知道这些事情”。
将性别定义为一种粗糙的二元性,以现有的染色体或特定的解剖结构为依据,可能会过于局限。一些种类,比如线虫秀丽隐杆线虫美国有一种性别只制造精子细胞,另一种性别同时制造精子和卵细胞。在大量的物种中,性别是由环境而不是染色体决定的。还有一些物种可以在一生中改变性别。在这种情况下,将细胞、组织甚至整个生物体归类为两类会遇到重重困难。
批评人士还认为,该政策存在一个后勤问题:包括两性将需要更多的动物。

《自然》杂志提高了研究中性别和性别报告的标准
伦敦帝国理工学院(Imperial College London)的遗传学家艾琳·米格尔-阿利亚加(Irene Miguel-Aliaga)说:“有一种假设是,如果你在做老鼠研究,你想考虑两种性别,你就必须把数量增加一倍。”她帮助制定了使用两种性别的命令由英国医学研究委员会在今年早些时候发起.她说,如果性别差异驱动了一项研究的假设,那么可能需要加倍,但为了探索目的,“你只需要有足够多的动物来判断你的发现是否与两性相关”。
平均而言,样本量可能需要增加多达三分之一才能达到这一标准6.位于马萨诸塞州波士顿的贝斯以色列女执事医疗中心内分泌学、糖尿病和代谢科主任埃文·罗森(Evan Rosen)说,问题在于“小鼠研究很昂贵,这种新立场的一个令人沮丧的方面是,NIH经常要求我们在雌性小鼠身上进行研究,但却不愿提供足够的资金”。
今年早些时候,他和他的团队发表了7对一种被称为白色脂肪组织的脂肪组织进行了广泛的人类和小鼠图谱研究,他们遇到了一个有趣的问题:该领域的大多数小鼠研究都是在雄性小鼠身上进行的,而雄性小鼠的脂肪含量往往比雌性小鼠多得多。相比之下,大多数人体样本都是在减肥手术中采集的,而在减肥手术中,女性患者占绝大多数。当他们开始绘制地图集时,他们意识到他们的小鼠和人类种群呈相反的方向倾斜,必须确保其中包括雌性小鼠和男性的组织。最后,罗森说:“我们确实看到了瘦人与肥胖者、瘦老鼠与肥胖老鼠之间的巨大差异,但性别作为比较指标的作用却失败了。”
米格尔-阿利亚加说,即使是这种没有差异的“负面”发现也具有信息量。她指出:“无论你研究的是什么,都没有显示出性别二态性,或者它可能导致的治疗方法可以适用于两性,这仍然是很好的。”做这些研究是“双赢”的。
起伏不平的路
这些政策旨在迫使人们做出改变,但许多科学家很难常规地遵守这些政策,或者在研究中适当地纳入性别因素。在电子邮件发送给自然克莱顿指出,到2015年,也就是NIH确立临床试验要求的22年后,由NIH资助的经评估的随机对照试验中,只有不到三分之一的试验按性别报告结果或为不这样做提供解释。2018年的一项回顾发现,在过去的14年里,这根针基本上没有动过8.
当女性被纳入试验时,其比例往往与该群体中某些疾病的现实患病率不符。2019年发表的一项研究发现,在作者从2014年到2018年分析的11种疾病类别中,女性在7种疾病中比例不足,包括肝脏和肾脏疾病9.
在动物和细胞研究中,新政策的依从性更不稳定。伊利诺伊州芝加哥市西北大学范伯格医学院医学社会科学系的SABV研究员妮可·沃伊托维奇(Nicole Woitowich)与人合著了一份报告10看看2009年至2019年动物研究中的性别包容是如何变化的。在34种期刊的9个研究领域中,她和她的同事们发现,包括两性在内的研究比例有所上升。但在其中8个领域,按性别进行的数据分析并没有增加,作者也很少解释这种遗漏(参见“性别研究的详细审查”)。
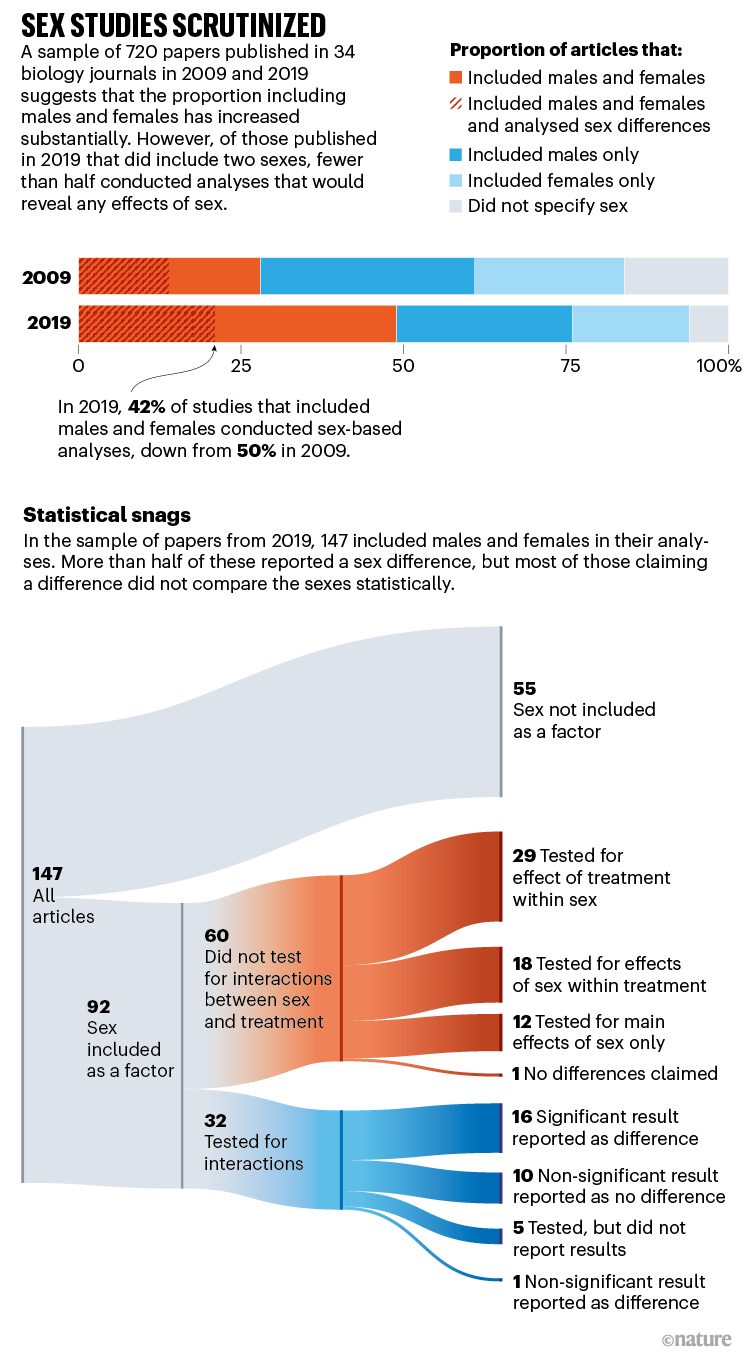
沃伊托维奇特别提到了神经科学。该领域的研究显示,将两种性别包括在内的人数大幅增加,但只有不到一半的人愿意为每一种性别详细说明数字。这是一个可重复性的问题。她说,性别包容“很好”,但“如果我们不做基于性别的分析,我们实际上就把一半的数据留在了桌面上”。
另一个小组的后续研究更仔细地观察了同一批研究是如何处理这些数据的11.他们中只有少数人按性别报告了数据,在那些报告了数据的人中,基于性别的分析是不恰当的——在70%的病例中,甚至没有比较性别之间的治疗效果——或者结果被误解了。
一个常见的错误是,如果一个结果在一种性别中显著而在另一种性别中不显著,即使两种性别没有直接比较,也会推断出基于性别的差异。例如,由于个体差异,一个组的值可能比另一组的值在平均值附近的范围更大。单独测试这些组的显著性并不能显示它们是否不同;它们必须使用统计检验相互比较。
但该报告也描述了相反的偏见:消除真实性效果的风险。当作者将性别作为分析的一个因素而不考虑性别时,这种风险就出现了,即使初步计算表明性别差异,他们有时也会这样做。
COVID-19再次提供了一个最近的例子,说明错误的分析可能会混淆洞察力。2020年报告12发现患有COVID-19的男性和女性之间的免疫和炎症相关分子水平存在差异。但是后续的分析13科学历史学家、马萨诸塞州剑桥市哈佛大学性别科学实验室主任莎拉·理查森(Sarah Richardson)和她的同事指出了分析中的错误。理查森和她的同事们写道,其中三个结果的差异是在同一性别内,而不是两性之间。例如,在女性中,一种信号分子的水平在基线时在病情恶化的人和病情保持稳定的人之间存在显著差异,但这种模式不适用于男性。
最初的作者得出的结论是,这一结果代表了“性别之间”的差异,尽管两种性别没有直接进行比较。相比之下,理查森和她的同事进行了直接比较,发现这两种差异并没有明显的区别,这表明性别没有作用。他们得出的结论是,一些原本归因于性别的差异可能是由性别和种族等社会因素造成的,而不是性别。
一些研究人员认为,在临床试验中应该考虑到这些社会因素。但这些变量更难衡量和整合。瑞士洛桑大学的社会学家玛德琳·佩普说,将性纳入国家卫生研究院政策优先事项的过程“对性别来说会困难得多,即使最终很难将性别和性别作为健康决定因素分开”。
Schiebinger的团队花了几年时间开发用于临床试验的性别问卷,希望NIH有朝一日能将性别作为一个社会文化变量。但她表示,这是在“等待更好的措施”。
SAGER的指导方针和出版商自己关于性别和性别的政策旨在鼓励作者包括并报告两性。但期刊对这些政策的遵守是零星的。2021年的一项非正式审查表明,一些期刊编辑继续抵制采用SABV政策,声称这些政策不适用于他们的领域14.
加州大学戴维斯分校(University of California, Davis)加州国家灵长类动物研究中心(California National Primate Research Center)的心理学家伊莉莎·布利斯-莫罗(Eliza Bliss-Moreau)说,人们对药物依从性差和吸收慢的抱怨并不出人意料。“人们不是特别擅长改变,”她指出。她还说,NIH资金周期的长度已经为政策追赶造成了滞后。“有很多东西被写入了政策,人们对此颇有怨言,但10年或15年后,事情就变成了这样。”
局部进展
尽管道路坎坷,但20世纪90年代初开始实施的联邦指导方针已经带来了一些重要的医学发现,这也许是一个信号,预示着几年后基础研究可能会出现关键的启示。
例如,心脏对几种药物(包括抗抑郁药和抗生素)的电反应存在基于性别的差异。因此,现在建议对某些药物进行基于性别的剂量调整2.
类固醇激素,如雌激素和雄激素,被认为是造成男女差异的主要因素。例如,女性代谢普萘洛尔(一种被称为β受体阻滞剂的降压药)的速度比男性慢15.研究人员认为,作用于肝脏的与性有关的类固醇激素可以发挥这些作用。其他因素还包括身体的大小和组成,比如脂肪和肌肉的比例,女性的比例往往更高。
男性和女性的风险界限也可能不同。2021年对与收缩压相关的心血管风险的分析显示,如果将两性的数据集中在一起,而不是进行适当的分析,会发生什么3..作者发现,当数据汇总时,风险增加的范围是收缩压120-129毫米汞柱(mmHg)。但针对性别的分析显示,对于女性来说,当收缩压超过110毫米汞柱时,患病风险实际上开始攀升。如果其他研究证实了这些发现,结果将是心血管疾病风险计算的巨大变化。
加州洛杉矶雪松西奈医疗中心的心脏病专家、该报告的资深作者苏珊·程(Susan Cheng)说,这项研究碰巧“在很大程度上受到了美国国家卫生研究院(NIH)关于健康结果性别差异的申请的启发和推动”。她说,如果没有呼吁专门设计研究来寻找性别差异,“我们有很多想法,但没有一个主题重点”。Cheng说,他们发现男性和女性在风险临界值上存在差异,这“实际上是一个真正的‘顿悟时刻’”。“我当时就想,‘我们以前怎么没发现呢?’”她将这一结果归因于美国国家卫生研究院的挑战。“他们促成了这一切。”

 《自然》杂志提高了研究中性别和性别报告的标准
《自然》杂志提高了研究中性别和性别报告的标准 为什么男女对疼痛的感觉不同
为什么男女对疼痛的感觉不同